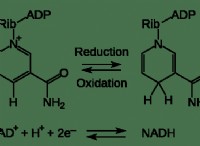
Πώς σπάζουν οι δεσμοί υδρογόνου;
1. Θερμοκρασία:
* Αυξημένη θερμοκρασία: Η θερμότητα παρέχει ενέργεια στα μόρια, αυξάνοντας την κινητική τους ενέργεια και προκαλώντας τους να δονείται πιο έντονα. Αυτή η δόνηση μπορεί να διαταράξει τους αδύναμους δεσμούς υδρογόνου, οδηγώντας στη θραύση τους. Αυτός είναι ο λόγος για τον οποίο πολλά μόρια με δεσμούς υδρογόνου, όπως το νερό, έχουν υψηλό σημείο βρασμού.
2. Διαλύτης:
* Πολικοί διαλύτες: Οι πολικοί διαλύτες μπορούν να διαταράξουν τους δεσμούς υδρογόνου ανταγωνίζοντας τα άτομα υδρογόνου. Για παράδειγμα, το νερό μπορεί να σχηματίσει δεσμούς υδρογόνου με τα άτομα υδρογόνου ενός άλλου μορίου, σπάζοντας αποτελεσματικά τον αρχικό δεσμό υδρογόνου.
* Μη πολικοί διαλύτες: Οι μη πολικοί διαλύτες μπορούν επίσης να διαταράξουν τους δεσμούς υδρογόνου, αλλά λιγότερο αποτελεσματικά. Το κάνουν αυτό μειώνοντας την πολικότητα του περιβάλλοντος, εξασθενίζοντας τις ηλεκτροστατικές αλληλεπιδράσεις που συγκρατούν τον δεσμό υδρογόνου μαζί.
3. ph:
* Αλλαγές στο ph: Η αλλαγή του ρΗ ενός διαλύματος μπορεί να επηρεάσει την κατανομή του φορτίου εντός των μορίων, επηρεάζοντας την αντοχή των δεσμών υδρογόνου. Για παράδειγμα, η προσθήκη οξέος μπορεί να πρωτονικά ένα μόριο, καθιστώντας λιγότερο πιθανό να συμμετάσχει στη δέσμευση υδρογόνου.
4. Πίεση:
* Αυξημένη πίεση: Ενώ είναι λιγότερο κοινή από τη θερμοκρασία, η αύξηση της πίεσης μπορεί επίσης να σπάσει δεσμούς υδρογόνου. Η συμπίεση που προκαλείται από την υψηλή πίεση μπορεί να μειώσει την απόσταση μεταξύ των μορίων, μειώνοντας τη αντοχή του δεσμού υδρογόνου και οδηγώντας στη θραύση του.
5. Μηχανική δύναμη:
* Μηχανική διέγερση ή διάτμηση: Οι ισχυρές φυσικές δυνάμεις μπορούν επίσης να διαταράξουν τους δεσμούς υδρογόνου. Αυτό είναι ιδιαίτερα σημαντικό σε καταστάσεις όπως η ανάμειξη των λύσεων ή η εφαρμογή μηχανικού στρες στα υλικά.
Η κατανόηση του πλαισίου είναι το κλειδί: Η συγκεκριμένη μέθοδος με την οποία το διάλειμμα των δεσμών υδρογόνου εξαρτάται από την συγκεκριμένη κατάσταση και τον τύπο των εμπλεκόμενων μορίων.
Για παράδειγμα, στα βιολογικά συστήματα, τα ένζυμα συχνά παίζουν ρόλο στη διάσπαση δεσμών υδρογόνου, διευκολύνοντας συγκεκριμένες αντιδράσεις. Στην επιστήμη των υλικών, οι ιδιότητες των πολυμερών επηρεάζονται από τη δύναμη και τη διάσπαση των δεσμών υδρογόνου μεταξύ των μορίων τους.