Διαφορά μεταξύ πίεσης ατμών και σημείου βρασμού
Κύρια διαφορά – Πίεση ατμών έναντι σημείου βρασμού
Η εξάτμιση και ο βρασμός είναι δύο όροι που χρησιμοποιούνται για να εκφράσουν την αλλαγή φάσης ενός υγρού ή ενός στερεού. Η εξάτμιση είναι η αλλαγή φάσης ενός υγρού ή στερεού στον ατμό του. Ο βρασμός προκαλεί την αλλαγή φάσης ενός υγρού στους ατμούς του. Η εξάτμιση προκαλεί την τάση ατμών ενός κλειστού συστήματος. Το σημείο βρασμού είναι η θερμοκρασία στην οποία ένα υγρό εξατμίζεται. Αν και αυτοί οι δύο όροι σχετίζονται μεταξύ τους, υπάρχουν διαφορές μεταξύ τους. Η κύρια διαφορά μεταξύ της πίεσης ατμών και του σημείου βρασμού είναι ότι η πίεση ατμών είναι μια μέτρηση της πίεσης ενώ το σημείο βρασμού είναι μια μέτρηση της θερμοκρασίας.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η πίεση ατμών
– Ορισμός, Προϋποθέσεις, Χαρακτηριστικά
2. Τι είναι το σημείο βρασμού
– Ορισμός, Χαρακτηριστικά
3. Ποια είναι η διαφορά μεταξύ της πίεσης ατμών και του σημείου βρασμού
– Σύγκριση βασικών διαφορών
Βασικοί όροι:ατμός, σημείο βρασμού, πίεση ατμών, κινητική ενέργεια, θερμοκρασία, ατμοσφαιρική πίεση 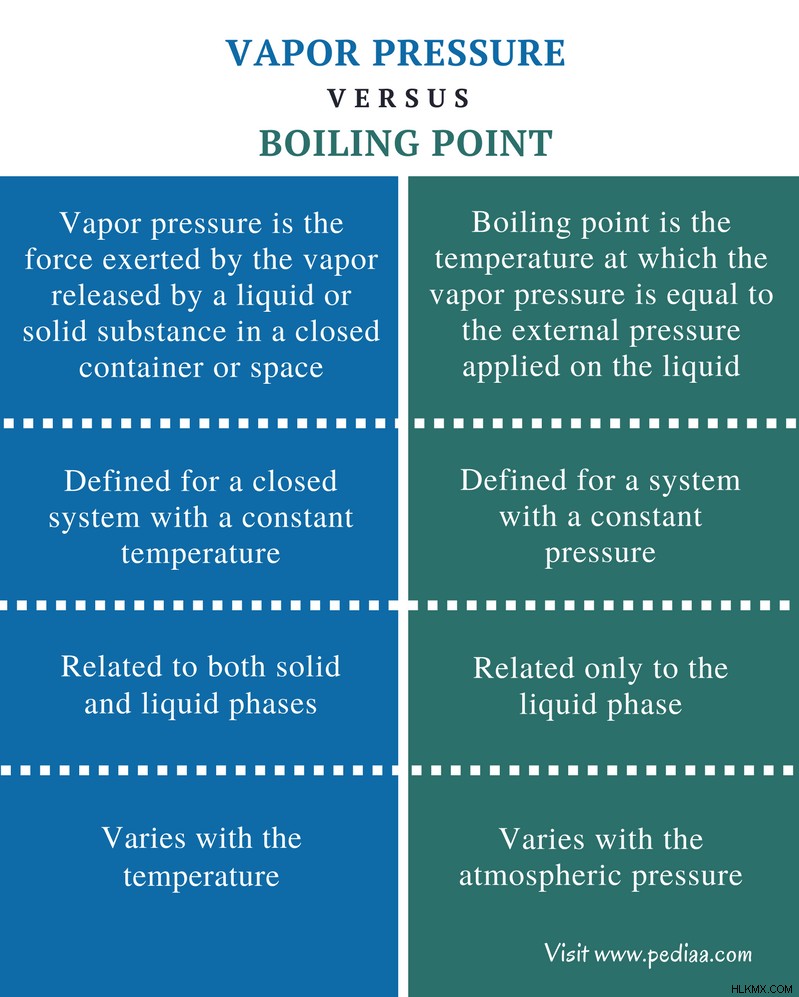
Τι είναι η πίεση ατμών;
Η πίεση ατμών μπορεί να οριστεί ως η δύναμη που ασκείται από τον ατμό. Ο ατμός πρέπει να πληροί τις ακόλουθες συνθήκες για να ασκήσει την πίεση ατμών.
- Ο ατμός πρέπει να βρίσκεται σε ισορροπία με την υγρή ή τη στερεή του φάση.
- Ο ατμός πρέπει να είναι σε σταθερή θερμοκρασία.
- Τόσο ο ατμός όσο και η συμπυκνωμένη του μορφή θα πρέπει να υπάρχουν σε ένα κλειστό σύστημα.
Η τάση ατμών σχετίζεται με την επιθυμία των μορίων να διαφύγουν από το υγρό ή το στερεό. Ως εκ τούτου, ουσίες με υψηλή τάση ατμών σε κανονική θερμοκρασία θεωρούνται πτητικές. Όσο η θερμοκρασία παραμένει σταθερή, η τάση ατμών παραμένει επίσης σταθερή. Μόλις όμως αυξηθεί η θερμοκρασία, αυξάνεται η κίνηση (κινητική ενέργεια) των μορίων του υγρού, απελευθερώνοντας όλο και περισσότερα μόρια από το υγρό. Ως αποτέλεσμα, η μετάβαση των υγρών μορίων σε ατμό αυξάνεται. Έτσι αυξάνεται και η τάση ατμών. Σε μια ορισμένη θερμοκρασία, η τάση ατμών γίνεται ίση με την εξωτερική πίεση που ασκείται στο υγρό ή το στερεό. Αυτή η θερμοκρασία ονομάζεται σημείο βρασμού του υγρού.

Εικόνα 1:Πίεση ατμών
Τι είναι το σημείο βρασμού;
Το σημείο βρασμού είναι η θερμοκρασία στην οποία βράζει ένα υγρό. Με άλλα λόγια, είναι η θερμοκρασία στην οποία η τάση ατμών ενός υγρού είναι ίση με την εξωτερική πίεση που ασκείται στο υγρό από το περιβάλλον.
Το σημείο βρασμού ενός υγρού ποικίλλει ανάλογα με την ατμοσφαιρική πίεση. Ως εκ τούτου, η τιμή του σημείου βρασμού για ένα συγκεκριμένο υγρό δεν είναι πάντα σταθερή. Η ατμοσφαιρική πίεση ποικίλλει ανάλογα με το υψόμετρο. Για παράδειγμα, το νερό συνήθως βράζει στους 100 C όταν η ατμοσφαιρική πίεση είναι 1 atm. Αλλά σε μεγαλύτερα υψόμετρα, το νερό βράζει σε χαμηλότερες θερμοκρασίες. Αυτό συμβαίνει επειδή η τάση ατμών πρέπει να είναι ίση με την ατμοσφαιρική πίεση για να βράσει ένα υγρό. Καθώς η πίεση σε μεγαλύτερα υψόμετρα είναι χαμηλότερη, αρκεί μια χαμηλή θερμική ενέργεια (θερμοκρασία) για να πληρούνται τα παραπάνω κριτήρια.
Ακόμη και σε θερμοκρασίες κάτω από το σημείο βρασμού, τα υγρά μόρια θα γίνουν ατμοί λόγω μιας διαδικασίας που ονομάζεται εξάτμιση. Η εξάτμιση είναι η διαφυγή υγρών μορίων που βρίσκονται στην επιφάνεια ενός υγρού. Αυτά τα μόρια συνδέονται μόνο χαλαρά με τα άλλα μόρια του υγρού. Έτσι, μπορούν εύκολα να αποκολληθούν από άλλα μόρια και να διαφύγουν από το υγρό ως ατμός. Αλλά στο βρασμό, τα μόρια που βρίσκονται οπουδήποτε στο υγρό μπορούν να διαφύγουν από το υγρό.

Εικόνα 02:Υδρατμοί που βγαίνουν από το άνοιγμα ενός βραστήρα
Διαφορά μεταξύ πίεσης ατμών και σημείου βρασμού
Ορισμός
Πίεση ατμών: Η πίεση ατμών είναι η δύναμη που ασκείται από τον ατμό που απελευθερώνεται από μια υγρή ή στερεή ουσία σε ένα κλειστό δοχείο ή χώρο.
Σημείο βρασμού: Σημείο βρασμού είναι η θερμοκρασία στην οποία η τάση ατμών είναι ίση με την εξωτερική πίεση που εφαρμόζεται στο υγρό.
Συγκεκριμένες συνθήκες
Πίεση ατμών: Η τάση ατμών ορίζεται για ένα κλειστό σύστημα με σταθερή θερμοκρασία.
Σημείο βρασμού: Το σημείο βρασμού ορίζεται για ένα σύστημα με σταθερή πίεση.
Φυσικές καταστάσεις
Πίεση ατμών: Η τάση ατμών σχετίζεται τόσο με τη στερεά όσο και με την υγρή φάση.
Σημείο βρασμού: Το σημείο βρασμού σχετίζεται μόνο με την υγρή φάση.
Παραλλαγές
Πίεση ατμών: Η πίεση ατμών ποικίλλει ανάλογα με τη θερμοκρασία.
Σημείο βρασμού: Το σημείο βρασμού ποικίλλει ανάλογα με την ατμοσφαιρική πίεση.
Συμπέρασμα
Η πίεση ατμών και το σημείο βρασμού είναι δύο σχετικοί όροι που χρησιμοποιούνται συχνά στη φυσική χημεία. Αν και η τάση ατμών σχετίζεται με το σημείο βρασμού, έχουν διαφορετικά χαρακτηριστικά. Η κύρια διαφορά μεταξύ της πίεσης ατμών και του σημείου βρασμού είναι ότι η τάση ατμών είναι μια μέτρηση της πίεσης ενώ το σημείο βρασμού είναι μια μέτρηση της θερμοκρασίας.