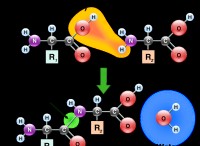
Ποια είναι η πλειοψηφία του αρνητικού φορτίου στο μόριο νερού;
Εδώ είναι γιατί:
* Το οξυγόνο είναι πιο ηλεκτροαρνητικό από το υδρογόνο: Το οξυγόνο έχει ισχυρότερη έλξη στα ηλεκτρόνια από το υδρογόνο. Αυτό σημαίνει ότι τα κοινόχρηστα ηλεκτρόνια στους δεσμούς O-H περνούν περισσότερο χρόνο πιο κοντά στο άτομο οξυγόνου.
* λυγισμένη μοριακή γεωμετρία: Το μόριο νερού έχει ένα λυγισμένο σχήμα λόγω των δύο μοναχικών ζευγών ηλεκτρονίων στο άτομο οξυγόνου. Αυτό το λυγισμένο σχήμα συγκεντρώνει περαιτέρω το αρνητικό φορτίο γύρω από το οξυγόνο.
Ως αποτέλεσμα, το άτομο οξυγόνου στο νερό φέρει ένα μερικό αρνητικό φορτίο (Δ-), ενώ τα άτομα υδρογόνου φέρουν μερικό θετικό φορτίο (δ+). Αυτό δημιουργεί ένα πολικό μόριο με μια διπολική στιγμή.