Τα οξέα ή οι βάσεις εξατμίζονται ταχύτερα;
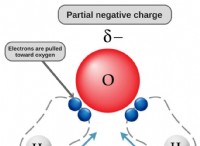
* Μοριακή δομή: Η δύναμη των διαμοριακών δυνάμεων μεταξύ των μορίων παίζει καθοριστικό ρόλο. Οι ισχυρότερες δυνάμεις (όπως η δέσμευση υδρογόνου) δυσκολεύουν να ξεφύγουν από τα μόρια στη φάση ατμών.
* Πίεση ατμών: Αυτή είναι η πίεση που ασκείται από τον ατμό μιας ουσίας σε ισορροπία με την υγρή φάση της. Η υψηλότερη πίεση ατμών σημαίνει ότι περισσότερα μόρια βρίσκονται στη φάση ατμών, οπότε η εξάτμιση είναι ταχύτερη.
* Θερμοκρασία: Οι υψηλότερες θερμοκρασίες παρέχουν περισσότερη ενέργεια στα μόρια, διευκολύνοντας τους να ξεπεράσουν τις ενδομοριακές δυνάμεις και να εξατμιστούν.
* επιφάνεια: Μια μεγαλύτερη επιφάνεια εκθέτει περισσότερα μόρια στον αέρα, αυξάνοντας τον ρυθμό εξάτμισης.
Εδώ είναι πώς αυτοί οι παράγοντες μπορούν να παίξουν με οξέα και βάσεις:
* Ισχυρά οξέα/βάσεις: Αυτά τείνουν να έχουν ισχυρές διαμοριακές δυνάμεις λόγω της υψηλής πολικότητάς τους, η οποία μπορεί να επιβραδύνει την εξάτμιση.
* αδύναμα οξέα/βάσεις: Αυτά μπορεί να έχουν ασθενέστερες διαμοριακές δυνάμεις, ενδεχομένως επιτρέποντας ταχύτερη εξάτμιση.
Παραδείγματα:
* Υδροχλωρικό οξύ (HCl): Ένα ισχυρό οξύ, έχει σχετικά υψηλή πίεση ατμών, καθιστώντας το εξαντλείται γρηγορότερα.
* Υδροξείδιο του νατρίου (NAOH): Μια ισχυρή βάση, έχει χαμηλότερη πίεση ατμών και μια πιο σύνθετη μοριακή δομή, οδηγώντας σε βραδύτερη εξάτμιση.
* οξικό οξύ (CH3COOH): Ένα αδύναμο οξύ, έχει σχετικά χαμηλή πίεση ατμών, αλλά το μικρότερο μοριακό του μέγεθος μπορεί να το κάνει να εξατμιστεί με αξιοπρεπή ρυθμό.
Συμπερασματικά, δεν είναι γενικός κανόνας ότι τα οξέα εξατμίζονται ταχύτερα από τις βάσεις ή το αντίστροφο. Το συγκεκριμένο οξύ ή η βάση και οι ιδιότητές του, μαζί με άλλους παράγοντες όπως η θερμοκρασία και η πίεση, καθορίζουν τον ρυθμό εξάτμισης.