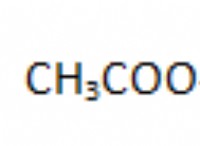Ποιο επιστημονικό συμπέρασμα μπορεί να γίνει σχετικά με το συνδυασμό χλωριούχου χαλκού και αλουμινόχαρτου;
αντίδραση:
* cucl₂ (aq) + 2Al (s) → 2alcl₃ (aq) + 3cu (s)
Επεξήγηση:
* αλουμίνιο (al) είναι πιο αντιδραστικό από το χαλκός (Cu) . Αυτό σημαίνει ότι το αλουμίνιο έχει ισχυρότερη τάση να χάνει ηλεκτρόνια και να σχηματίζει θετικά ιόντα.
* Στην αντίδραση, τα άτομα αλουμινίου μετατοπίζουν ιόντα χαλκού από το διάλυμα χλωριούχου χαλκού.
* Τα άτομα αλουμινίου χάνουν ηλεκτρόνια και σχηματίζουν ιόντα αλουμινίου (al³⁺), τα οποία στη συνέχεια συνδυάζονται με ιόντα χλωριούχου (CL⁻) για να σχηματίσουν χλωριούχο αλουμινίου (ALCL₃).
* Τα ιόντα χαλκού (Cu²) κερδίζουν ηλεκτρόνια και γίνονται άτομα χαλκού (Cu), τα οποία καταβυθίζονται έξω από το διάλυμα ως κόκκινο-καφέ στερεό.
Παρατηρήσεις:
* Θα παρατηρήσετε μια αλλαγή χρώματος στο διάλυμα, καθώς το διάλυμα χλωριούχου μπλε χαλκού γίνεται σαφής ή ελαφρώς κιτρινωπή.
* Θα δείτε επίσης ένα κοκκινωπό-καφέ επικάλυψη που σχηματίζεται στο αλουμινόχαρτο, το οποίο είναι το εναποτιθέμενο μεταλλικό χαλκό.
* Η αντίδραση είναι εξωθερμική, που σημαίνει ότι απελευθερώνει τη θερμότητα και το διάλυμα μπορεί να αισθάνεται ζεστό.
επιστημονικό συμπέρασμα:
* Αυτή η αντίδραση καταδεικνύει τη σχετική αντιδραστικότητα των μετάλλων. Το αλουμίνιο, που είναι πιο αντιδραστικό, μετατοπίζει χαλκό από την ένωση.
* Η αντίδραση μεμονωμένης μετατόπισης παράγει μια νέα ένωση (χλωριούχο αλουμίνιο) και ένα νέο στοιχείο (χαλκός).
* Η αντίδραση είναι ένα σαφές παράδειγμα μιας αντίδρασης redox (αντίδραση οξείδωσης-μείωσης), όπου τα ηλεκτρόνια μεταφέρονται από αλουμίνιο σε χαλκό.
Πρόσθετες σημειώσεις:
* Η αντίδραση χρησιμοποιείται συχνά σε εισαγωγικά εργαστήρια χημείας για να επιδείξει αντιδράσεις μεμονωμένης μετατόπισης και την έννοια της σειράς αντιδραστικότητας.
* Η ποσότητα που εναποτίθεται από χαλκό εξαρτάται από την ποσότητα του χλωριούχου χλωριούχου που χρησιμοποιείται και την επιφάνεια του αλουμινίου αλουμινίου.
* Η αντίδραση μπορεί να είναι αρκετά έντονη, οπότε είναι σημαντικό να την εκτελέσετε σε ένα ασφαλές περιβάλλον, με κατάλληλες προφυλάξεις ασφαλείας.