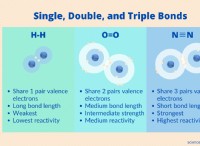
Γιατί τα άτομα βρωμίου είναι τόσο δραστικά;
* Διαμόρφωση ηλεκτρονίων: Το βρώμιο έχει 7 ηλεκτρόνια σθένους (ηλεκτρόνια στο εξώτατο κέλυφος). Θέλει να έχει ένα πλήρες εξωτερικό κέλυφος 8 ηλεκτρονίων για σταθερότητα, παρόμοια με τα ευγενή αέρια. Για να επιτευχθεί αυτό, το βρώμιο κερδίζει εύκολα ένα ηλεκτρόνιο για να σχηματίσει ένα ιόν βρωμιδίου (Br-).
* Ηλεκτροργατιστικότητα: Το βρώμιο έχει σχετικά υψηλή ηλεκτροαρνητικότητα, που σημαίνει ότι προσελκύει έντονα ηλεκτρόνια. Αυτό καθιστά πιθανό να τραβήξει ηλεκτρόνια μακριά από άλλα άτομα σε χημική αντίδραση.
* Μικρή ατομική ακτίνα: Το βρώμιο έχει μικρότερη ατομική ακτίνα σε σύγκριση με μεγαλύτερα αλογόνα όπως το ιώδιο. Αυτό σημαίνει ότι τα ηλεκτρόνια στο εξωτερικό του κέλυφος κρατούνται πιο σφιχτά από τον πυρήνα και προσελκύονται ευκολότερα από άλλα άτομα.
Αυτοί οι παράγοντες συμβάλλουν στην υψηλή αντιδραστικότητα του βρωμίου. Συμμετέχει εύκολα σε αντιδράσεις για να κερδίσει ένα ηλεκτρόνιο και να επιτύχει μια σταθερή διαμόρφωση οκτάδων.