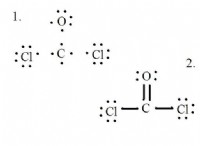Γιατί μπορούν μόνο τέσσερα άτομα φωσφόρου να παράγουν δύο μόρια τριοξείδιο του διφωσόρου, ακόμη και όταν υπάρχει υπερβολικά άτομα οξυγόνου;
Εδώ είναι γιατί:
* Stoichiometry: Η ισορροπημένη χημική εξίσωση για την αντίδραση μεταξύ φωσφόρου και οξυγόνου για να σχηματιστεί τριαξείδιο του διφωσφοριού είναι:
4 p + 3 o₂ → 2 p₂o₃
* Η εξίσωση εξηγεί όλα: Αυτή η εξίσωση δείχνει ότι 4 moles του φωσφόρου (Ρ) αντιδρούν με 3 moles οξυγόνου (O₂) για να παράγουν 2 γραμμομονείς του τριαξειδίου του διφωσφοριού (P₂O₃).
* Η υπερβολική οξυγόνο δεν αλλάζει την αναλογία: Ακόμη και αν έχετε μια περίσσεια οξυγόνου, η αντίδραση θα καταναλώνει μόνο 3 γραμμομονείς Οο για κάθε 4 γραμμομόρια του P. Η περίσσεια οξυγόνου παραμένει μη αντιδράσει.
Εν ολίγοις: Ενώ υπάρχει υπερβολική οξυγόνο, δεν αλλάζει τη θεμελιώδη αναλογία αντιδραστηρίων και προϊόντων που υπαγορεύονται από την ισορροπημένη χημική εξίσωση. Η αντίδραση θα παράγει ακόμα 2 γραμμομορείς τριαξειδίου του διφωσφοριού για κάθε 4 γραμμομορείς φωσφόρου που χρησιμοποιείται, ανεξάρτητα από την ποσότητα του οξυγόνου που είναι διαθέσιμο.