Ποιο είναι το ταχύτερα κινούμενο μόριο αερίου;
Εδώ είναι γιατί:
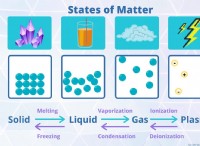
* Κινητική μοριακή θεωρία: Η ταχύτητα των μορίων αερίου σχετίζεται άμεσα με τη θερμοκρασία τους. Όσο υψηλότερη είναι η θερμοκρασία, τόσο ταχύτερα κινούνται τα μόρια.
* Μοριακή μάζα: Τα ελαφρύτερα μόρια κινούνται ταχύτερα από τα βαρύτερα στην ίδια θερμοκρασία.
Για να προσδιορίσετε το ταχύτερα κινούμενο μόριο αερίου, θα χρειαστεί:
1. Γνωρίστε τη θερμοκρασία: Όσο υψηλότερη είναι η θερμοκρασία, τόσο ταχύτερα όλα τα μόρια θα κινηθούν.
2. Εξετάστε τη μοριακή μάζα: Τα ελαφρύτερα μόρια όπως το υδρογόνο (H₂) θα κινούνται γενικά ταχύτερα από τα βαρύτερα μόρια όπως το οξυγόνο (O₂).
Παράδειγμα:
Σε μια δεδομένη θερμοκρασία, το αέριο υδρογόνου (H₂) θα είναι το ταχύτερο κινούμενο επειδή έχει τη χαμηλότερη μοριακή μάζα. Ωστόσο, εάν αυξήσετε τη θερμοκρασία ενός βαρύτερου αερίου όπως το Xenon (XE), θα μπορούσε ενδεχομένως να μετακινηθεί γρηγορότερα από το υδρογόνο σε χαμηλότερη θερμοκρασία.
Key Takeaway: Το ταχύτερα κινούμενο μόριο αερίου εξαρτάται τόσο από τη θερμοκρασία όσο και από τη μοριακή μάζα.