Διαφορά μεταξύ αμυλόζης και αμυλοπηκτίνης
Κύρια διαφορά – Αμυλόζη έναντι Αμυλοπηκτίνης
Το άμυλο είναι μια άχρωμη και άοσμη στερεή ουσία που μπορεί να βρεθεί στα φυτά ως υδατάνθρακας αποθήκευσης. Το άμυλο είναι πολυσακχαρίτης. Αποτελείται από έναν αριθμό μονομερών γλυκόζης. Αυτά τα μόρια γλυκόζης συνδέονται μεταξύ τους μέσω γλυκοσιδικών δεσμών για να σχηματίσουν πολυσακχαρίτη. Το άμυλο αποτελείται από δύο τύπους μορίων γνωστά ως αμυλόζη και αμυλοπηκτίνη. Τα μόρια αμυλόζης σχηματίζονται από πολλές μονάδες γλυκόζης διατεταγμένες με γραμμικό τρόπο. Η αμυλοπηκτίνη σχηματίζεται από πολλές μονάδες γλυκόζης διατεταγμένες με διακλαδισμένο τρόπο Αυτή είναι η βασική διαφορά μεταξύ των μορίων αμυλόζης και αμυλοπηκτίνης που υπάρχουν στο άμυλο.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η Αμυλόζη
– Ορισμός, Εμφάνιση και Αντιδράσεις
2. Τι είναι η Αμυλοπηκτίνη
– Ορισμός, Εμφάνιση και Αντιδράσεις
3. Ποιες είναι οι ομοιότητες μεταξύ της αμυλόζης και της αμυλοπηκτίνης
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ της αμυλόζης και της αμυλοπηκτίνης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:αμυλοπηκτίνη, αμυλόζη, γλυκοσιδικοί δεσμοί, γλυκόζη, μονοσακχαρίτης, πολυσακχαρίτης, άμυλο 
Τι είναι η Αμυλόζη
Η αμυλόζη είναι ένα ευθείας αλυσίδας πολυμερές μονάδων D-γλυκόζης. Είναι ένας πολυσακχαρίτης που αποτελείται από πολλές μονάδες μονοσακχαρίτη. Ο μονοσακχαρίτης που εμπλέκεται στο σχηματισμό της αμυλόζης είναι η D-γλυκόζη. Επομένως, η αμυλόζη θεωρείται πολυμερές.
20-25% της περιεκτικότητας σε άμυλο είναι αμυλόζη. Ο τύπος του χημικού δεσμού που υπάρχει μεταξύ των μονομερών γλυκόζης ονομάζεται α 1-4 γλυκοσιδικός δεσμός. Αυτό συμβαίνει επειδή η ομάδα ΟΗ που συνδέεται με τον πρώτο άνθρακα ενός μορίου γλυκόζης απομακρύνεται μαζί με ένα άτομο Η που συνδέεται με τον τέταρτο άνθρακα ενός άλλου μορίου γλυκόζης στο σχηματισμό αμυλόζης. Αυτό είναι γνωστό ως αντίδραση συμπύκνωσης, καθώς η αφαιρεθείσα ομάδα ΟΗ και το άτομο Η μαζί σχηματίζουν ένα μόριο νερού.
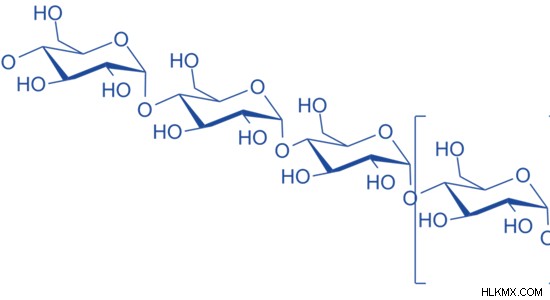
Εικόνα 1:Τρισδιάστατη προβολή αμυλόζης
Όταν προστίθεται διάλυμα ιωδίου στο άμυλο, μετατρέπεται σε σκούρο μπλε/μαύρο χρώμα. Αυτή η αλλαγή χρώματος δίνεται από την αμυλόζη που υπάρχει στο άμυλο μαζί με την αμυλοπηκτίνη. Η αμυλόζη είναι πιο διαλυτή στο νερό από την αμυλοπηκτίνη. Η αμυλόζη μπορεί να υδρολυθεί σε μονάδες γλυκόζης από ένζυμα όπως η α αμυλάση και η β αμυλάση.
Τι είναι η Αμυλοπηκτίνη
Η αμυλοπηκτίνη είναι ένα πολυμερές διακλαδισμένης αλυσίδας μονάδων D-γλυκόζης. Είναι ένας πολυσακχαρίτης που αποτελείται από μονοσακχαρίτες. Οι μονοσακχαρίτες είναι μόρια D-γλυκόζης. Το άμυλο περιέχει περίπου 80% αμυλοπηκτίνη.
Τα μόρια αμυλοπηκτίνης αποτελούνται από μονάδες γλυκόζης που συνδέονται μεταξύ τους μέσω α 1-4 γλυκοσιδικών δεσμών και α 1-6 γλυκοσιδικών δεσμών. Αυτοί οι α 1-6 γλυκοσιδικοί δεσμοί προκαλούν τη διακλαδισμένη δομή της αμυλοπηκτίνης. Εδώ, τα μόρια γλυκόζης συνδέονται μεταξύ τους μέσω του τέταρτου ατόμου άνθρακα καθώς και του έκτου ατόμου άνθρακα.
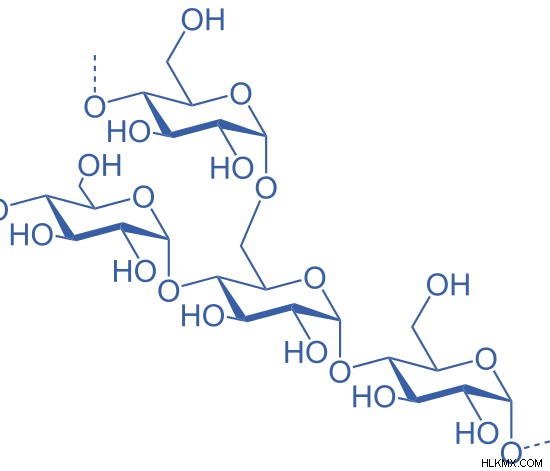
Εικόνα 2:Διακλάδωση στην Αμυλοπηκτίνη
Η αλλαγή χρώματος που δίνεται από την αμυλοπηκτίνη όταν προστίθεται διάλυμα ιωδίου είναι κοκκινοκαφέ χρώμα. Παρουσία ενζύμων α αμυλάσης και β αμυλάσης, οι γλυκοσιδικοί δεσμοί α 1-4 μπορούν να υδρολυθούν αλλά οι γλυκοσιδικοί δεσμοί α 1-6 δεν μπορούν να υδρολυθούν.
Η αμυλοπηκτίνη είναι λιγότερο διαλυτή στο νερό. Αλλά η αμυλοπηκτίνη είναι διαλυτή σε ζεστό νερό με πρήξιμο. Μπορεί από τζελ ή πάστα αμύλου όταν κρυώσει.
Ομοιότητες μεταξύ αμυλόζης και αμυλοπηκτίνης
- Και τα δύο είναι μόρια πολυσακχαριτών.
- Και τα δύο αποτελούνται από μονάδες D-γλυκόζης.
- Και τα δύο μόρια έχουν α 1-4 γλυκοσιδικούς δεσμούς.
- Και οι δύο τύποι βρίσκονται σε κόκκους αμύλου.
Διαφορά μεταξύ αμυλόζης και αμυλοπηκτίνης
Ορισμός
Αμυλόζη: Η αμυλόζη είναι ένα πολυμερές ευθείας αλυσίδας μονάδων D-γλυκόζης.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη είναι ένα πολυμερές διακλαδισμένης αλυσίδας μονάδων D-γλυκόζης.
Ποσοστό σε άμυλο
Αμυλόζη: Η περιεκτικότητα σε αμυλόζη στο άμυλο είναι περίπου 20%.
Αμυλοπηκτίνη: Η περιεκτικότητα σε αμυλοπηκτίνη στο άμυλο είναι περίπου 80%.
Δομή
Αμυλόζη: Η αμυλόζη είναι μια δομή ευθείας αλυσίδας.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη είναι μια διακλαδισμένη δομή.
Γλυκοσιδικοί δεσμοί
Αμυλόζη: Η αμυλόζη έχει α 1-4 γλυκοσιδικούς δεσμούς.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη έχει α 1-4 γλυκοσιδικούς δεσμούς και α 1-6 γλυκοσιδικούς δεσμούς.
Διαλυτότητα στο νερό
Αμυλόζη: Η αμυλόζη είναι λιγότερο διαλυτή στο νερό.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη είναι πιο διαλυτή στο νερό.
Αλλαγή χρώματος με ιώδιο
Αμυλόζη: Η αμυλόζη δίνει ένα σκούρο μπλε/μαύρο χρώμα όταν προστίθεται διάλυμα ιωδίου.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη δίνει ένα κοκκινωπό καφέ χρώμα όταν προστίθεται διάλυμα ιωδίου.
Υδρόλυση με ένζυμα
Αμυλόζη: Η αμυλόζη μπορεί να υδρολυθεί πλήρως με τα ένζυμα α αμυλάση και β αμυλάση.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη δεν μπορεί να υδρολυθεί πλήρως με τα ένζυμα α αμυλάση και β αμυλάση.
Σχηματισμός γέλης
Αμυλόζη: Η αμυλόζη δεν σχηματίζει γέλη όταν προστίθεται ζεστό νερό.
Αμυλοπηκτίνη: Η αμυλοπηκτίνη σχηματίζει ένα πήκτωμα όταν προστίθεται ζεστό νερό.
Συμπέρασμα
Η αμυλόζη και η αμυλοπηκτίνη είναι δύο τύποι πολυσακχαριτών που μπορούν να βρεθούν σε κόκκους αμύλου. Έχουν τόσο δομικές και χημικές διαφορές όσο και ομοιότητες. Η κύρια διαφορά μεταξύ της αμυλόζης και της αμυλοπηκτίνης είναι ότι η αμυλόζη είναι ένα πολυμερές ευθείας αλυσίδας ενώ η αμυλοπηκτίνη είναι ένα πολυμερές διακλαδισμένης αλυσίδας.