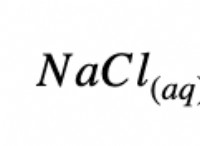Γιατί πρέπει να είστε προσεκτικοί όταν θερμαίνετε το διάλυμα NaCl για να εξατμίσετε νερό;
1. Spattering: Καθώς το νερό εξατμίζεται, το διάλυμα γίνεται όλο και περισσότερο συγκεντρωμένο. Αυτό το συμπυκνωμένο διάλυμα άλατος μπορεί εύκολα να πιτσιλιστεί λόγω:
* Ανύψωση σημείου βρασμού: Η προσθήκη αλατιού στο νερό αυξάνει το σημείο βρασμού του. Αυτό σημαίνει ότι η λύση θα είναι θερμότερη από το καθαρό νερό στο σημείο βρασμού του, αυξάνοντας τις δυνατότητες βίαιης βρασμού και ψεκασμού.
* υπερθέρμανση: Εάν το διάλυμα θερμαίνεται πολύ γρήγορα ή άνισα, το νερό μπορεί να υπερθερμανθεί. Αυτό σημαίνει ότι φτάνει σε μια θερμοκρασία πάνω από το σημείο βρασμού χωρίς να βράσει πραγματικά. Οποιαδήποτε διαταραχή μπορεί στη συνέχεια να προκαλέσει ξαφνικά το νερό να βράσει εκρηκτικά, οδηγώντας σε ψεκασμό.
2. Κρυσταλλοποίηση και "χτύπημα": Καθώς το διάλυμα συνεχίζει να εξατμίζεται, η συγκέντρωση άλατος αυξάνεται περαιτέρω. Όταν το διάλυμα γίνει υπερκορεσμένο, οι κρύσταλλοι αλατιού μπορούν να αρχίσουν να σχηματίζουν. Αυτοί οι κρύσταλλοι μπορούν να δράσουν ως θέσεις πυρήνωσης, προκαλώντας το υπόλοιπο νερό να βράσει ταχέως και ενδεχομένως "χτύπημα" ή να εκραγεί από το δοχείο.
3. Δυναμικό για εγκαύματα: Το θερμαινόμενο διάλυμα και κάθε ψεκασμό μπορεί να προκαλέσει σοβαρές εγκαύματα.
Προφυλάξεις ασφαλείας:
* Χρησιμοποιήστε τα κατάλληλα γυαλικά: Ένα ποτήρι με μεγάλη επιφάνεια προτιμάται για να επιτρέψει ακόμη και θέρμανση και να ελαχιστοποιηθεί η εκτόξευση.
* Θερμάνετε απαλά και αργά: Αποφύγετε την ταχεία θέρμανση για να αποφύγετε υπερθέρμανση.
* Χρησιμοποιήστε μια ράβδο ανάδευσης: Ανακατέψτε συνεχώς το διάλυμα για να εξασφαλίσετε ομοιόμορφη θέρμανση και να αποτρέψετε τη διαμόρφωση κρυστάλλων αλατιού.
* Χρησιμοποιήστε μια καυτή πλάκα με μαγνητικό αναδευτήρα: Αυτό μπορεί να βοηθήσει στην πρόληψη της πρόσκρουσης και να εξασφαλίσει ακόμη και θέρμανση.
* Φορέστε κατάλληλα προστατευτικά εργαλεία: Τα γυαλιά και τα γάντια ασφαλείας είναι απαραίτητα για να προστατεύσουν τα μάτια και το δέρμα σας.
* Εργαστείτε σε μια καλά αεριζόμενη περιοχή: Οι καπνοί από το θερμαινόμενο διάλυμα μπορεί να είναι ενοχλητικοί.
Λαμβάνοντας αυτές τις προφυλάξεις, μπορείτε να εξαντλήσετε με ασφάλεια και αποτελεσματικά το νερό από ένα διάλυμα NaCl.