Ποιος ιοντικός δεσμός προέρχεται από ασβέστιο και χλώριο;
* ασβέστιο (ca) είναι ένα μέταλλο στην ομάδα 2 του περιοδικού πίνακα, που σημαίνει ότι έχει 2 ηλεκτρόνια σθένους. Τείνει να χάσει αυτά τα ηλεκτρόνια για να επιτύχει μια σταθερή διαμόρφωση ηλεκτρονίων.
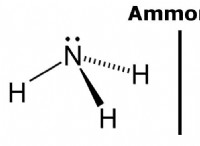
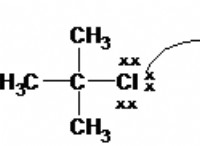
* χλώριο (cl) είναι μη μέταλλο στην ομάδα 17 του περιοδικού πίνακα, που σημαίνει ότι έχει 7 ηλεκτρόνια σθένους. Έχει την τάση να κερδίσει ένα ηλεκτρόνιο για να επιτύχει μια σταθερή διαμόρφωση ηλεκτρονίων.
Σχηματισμός του δεσμού:
1. Το ασβέστιο χάνει τα δύο ηλεκτρόνια σθένους να γίνει θετικά φορτισμένο ιόν ασβέστιο (Ca2⁺).
2. Δύο άτομα χλωρίου κάθε κέρδος ένα ηλεκτρόνιο να γίνουν αρνητικά φορτισμένα ιόντα χλωριούχου (CL⁻).
3. Οι αντίθετες χρεώσεις του ασβεστίου και των ιόντων χλωριούχου προσελκύουν ο ένας τον άλλον, σχηματίζοντας έναν ιοντικό δεσμό.
Η προκύπτουσα φόρμουλα είναι CaCl₂ επειδή απαιτούνται δύο ιόντα χλωριούχου για την εξισορρόπηση του φορτίου +2 του ιόντος ασβεστίου