Ποια στοιχεία αναμένετε να χάσετε ηλεκτρόνια στις χημικές τους αντιδράσεις κερδίζουν al sn br se;
* Κατανόηση της απώλειας ηλεκτρονίων
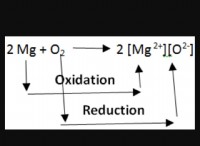
Η απώλεια ηλεκτρόνων σημαίνει ότι ένα στοιχείο γίνεται θετικά φορτισμένο (κατιόν). Αυτό συμβαίνει όταν ένα στοιχείο έχει σχετικά αδύναμη συγκράτηση στα εξωτερικά του ηλεκτρόνια. Αυτό συνήθως συνδέεται με τα μέταλλα.
* Περιοδικές τάσεις
* Ηλεκτροργατιστικότητα: Η ηλεκτροαρνητικότητα είναι ένα μέτρο της ικανότητας ενός ατόμου να προσελκύει ηλεκτρόνια. Τα μέταλλα τείνουν να έχουν χαμηλότερες τιμές ηλεκτροαρνητικότητας.
* ενέργεια ιονισμού: Η ενέργεια ιονισμού είναι η ενέργεια που απαιτείται για την απομάκρυνση ενός ηλεκτρονίου από ένα άτομο. Τα μέταλλα έχουν γενικά τις ενέργειες χαμηλότερης ιονισμού, καθιστώντας ευκολότερη την απομάκρυνση των ηλεκτρονίων.
Ανάλυση των στοιχείων
* al (αλουμίνιο): Ένα μέταλλο, χαμηλή ηλεκτροαρνητικότητα και ενέργεια χαμηλής ιονισμού. al είναι πιθανό να χάσει ηλεκτρόνια.
* sn (κασσίτερος): Ένα μέταλλο, αλλά λιγότερο αντιδραστικό από το αλουμίνιο. sn είναι λιγότερο πιθανό να χάσει ηλεκτρόνια από το AL, αλλά εξακολουθεί να μπορεί υπό ορισμένες συνθήκες.
* BR (βρωμίμιο): Μη μέταλλο, υψηλή ηλεκτροαρνητικότητα και ενέργεια υψηλής ιονισμού. br είναι πιθανό να κερδίσει ηλεκτρόνια.
* SE (Selenium): Μη μέταλλο, υψηλή ηλεκτροαρνητικότητα και ενέργεια υψηλής ιονισμού. se είναι πιθανό να κερδίσει ηλεκτρόνια.
Συμπέρασμα
* αλουμίνιο (al) και κασσίτερος (SN) είναι τα στοιχεία που είναι πιθανότερο να χάσουν ηλεκτρόνια σε χημικές αντιδράσεις.