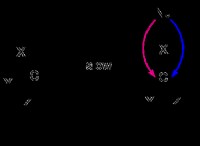
Ποιοι μεταλλικοί δεσμοί περιλαμβάνουν;
1. Απομακρυσμένα ηλεκτρόνια:
- Σε ένα μεταλλικό στερεό, τα ηλεκτρόνια σθένους των μεταλλικών ατόμων δεν συνδέονται στενά με κάποιο συγκεκριμένο άτομο. Είναι ελεύθεροι να κινούνται σε ολόκληρη τη δομή, σχηματίζοντας μια "θάλασσα" από απομακρυσμένα ηλεκτρόνια.
2. Θετικά ιόντα:
- Τα μεταλλικά άτομα χάνουν τα ηλεκτρόνια σθένους τους, καθιστώντας θετικά φορτισμένα ιόντα (κατιόντα). Αυτά τα ιόντα είναι διατεταγμένα σε ένα κανονικό, κρυσταλλικό πλέγμα.
3. Ισχυρή ηλεκτροστατική έλξη:
- Τα απομακρυσμένα ηλεκτρόνια προσελκύονται από τα θετικά μεταλλικά ιόντα, δημιουργώντας ισχυρές ηλεκτροστατικές δυνάμεις που συγκρατούν ολόκληρη τη δομή μαζί.
4. Υψηλή αγωγιμότητα:
- Η ελεύθερη κίνηση των ηλεκτρονίων επιτρέπει στα μέταλλα να διεξάγουν ηλεκτρική ενέργεια και να θερμανθούν πολύ καλά.
5. Μαλλιδοφυτότητα και ολκιμότητα:
- Τα απομακρυσμένα ηλεκτρόνια επιτρέπουν στα μεταλλικά άτομα να γλιστρούν μεταξύ τους χωρίς να σπάσουν τους μεταλλικούς δεσμούς, καθιστώντας τα μέταλλα εύπλαστα (μπορεί να σφυρηλατηθεί σε λεπτές φύλλα) και όλκιμων (μπορεί να τραβηχτεί σε καλώδια).
6. Luster:
- Τα απομακρυσμένα ηλεκτρόνια μπορούν να απορροφήσουν και να εκπέμπουν ξανά το φως, δίνοντας στα μέταλλα τη χαρακτηριστική τους λάμψη.
7. Υψηλά σημεία τήξης και βρασμού:
- Τα ισχυρά ηλεκτροστατικά αξιοθέατα μεταξύ των θετικών ιόντων και των απομακρυσμένων ηλεκτρόνων απαιτούν πολλή ενέργεια για να σπάσουν, οδηγώντας σε υψηλά σημεία τήξης και βρασμού.
Στην ουσία, η μεταλλική δέσμευση είναι μια ισχυρή ηλεκτροστατική έλξη μεταξύ ενός πλέγματος θετικών μεταλλικών ιόντων και μιας "θάλασσας" των απομακρυσμένων ηλεκτρονίων. Αυτός ο μοναδικός μηχανισμός συγκόλλησης δίνει στα μέταλλα τις ξεχωριστές ιδιότητές τους.