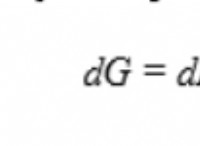Ποια εξίσωση δείχνει τη διατήρηση των ατόμων;
Δείτε πώς λειτουργεί:
1. Χημικές αντιδράσεις: Οι χημικές αντιδράσεις περιλαμβάνουν την αναδιάταξη των ατόμων εντός των μορίων. Τα άτομα δεν δημιουργούνται ούτε καταστρέφονται κατά τη διάρκεια αυτών των αναδιατάξεων.
2. Ισορροπημένες χημικές εξισώσεις: Αυτές οι εξισώσεις αντιπροσωπεύουν τις αλλαγές που συμβαίνουν κατά τη διάρκεια μιας χημικής αντίδρασης. Εξασφαλίζουν ότι ο αριθμός των ατόμων κάθε στοιχείου στην πλευρά του αντιδραστηρίου (τα υλικά εκκίνησης) είναι ίσος με τον αριθμό των ατόμων κάθε στοιχείου στην πλευρά του προϊόντος (οι ουσίες που σχηματίζονται).
Παράδειγμα:
Η καύση του μεθανίου (CH₄) αντιπροσωπεύεται από την ακόλουθη ισορροπημένη εξίσωση:
Ch₄ + 2o₂ → co₂ + 2h₂o
* Αντιδραστήρια: 1 άτομο άνθρακα (C), 4 άτομα υδρογόνου (Η) και 4 άτομα οξυγόνου (Ο)
* Προϊόντα: 1 άτομο άνθρακα (C), 4 άτομα υδρογόνου (Η) και 4 άτομα οξυγόνου (Ο)
Παρατηρήστε πώς ο αριθμός κάθε τύπου ατόμου παραμένει ο ίδιος και στις δύο πλευρές της εξίσωσης. Αυτό καταδεικνύει την αρχή της διατήρησης των ατόμων.
Βασικά σημεία:
* Η διατήρηση των ατόμων αποτελεί θεμελιώδη αρχή στη χημεία.
* Οι ισορροπημένες χημικές εξισώσεις εξασφαλίζουν τη διατήρηση των ατόμων.
* Η αρχή ισχύει για όλες τις χημικές αντιδράσεις.
Επομένως, η διατήρηση των ατόμων δεν αντιπροσωπεύεται από μια ενιαία εξίσωση, αλλά από την έννοια της εξισορρόπησης των χημικών εξισώσεων.