Είναι το SF3 ιοντικό ή ομοιοπολικό;
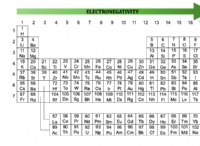
* Ηλεκτροργατιστικότητα: Το θείο και το φθόριο (F) είναι και τα δύο μέταλλα. Το φθόριο είναι το πιο ηλεκτροαρνητικό στοιχείο, που σημαίνει ότι έχει ισχυρή έλξη για τα ηλεκτρόνια. Ενώ η διαφορά ηλεκτροαρνητικότητας μεταξύ θείου και φθορίου είναι αρκετά μεγάλη ώστε να δημιουργήσει έναν πολικό ομοιοπολικό δεσμό, δεν είναι αρκετά μεγάλο για να σχηματίσει έναν ιοντικό δεσμό.
* Συγκέντρωση φύσης: Σε ομοιοπολικές ενώσεις, τα άτομα μοιράζονται ηλεκτρόνια για να επιτύχουν σταθερή διαμόρφωση ηλεκτρονίων. Στο SF3, το Atom Sulphur μοιράζεται ηλεκτρόνια με τρία άτομα φθορίου για να σχηματίσει τρεις ομοιοπολικούς δεσμούς.
* Δομή: Το SF3 έχει ένα πυραμιδικό σχήμα, το οποίο είναι χαρακτηριστικό των ομοιοπολικών ενώσεων με μοναχικά ζεύγη ηλεκτρονίων στο κεντρικό άτομο.
Συνοψίζοντας: Το SF3 είναι μια ομοιοπολική ένωση λόγω της κατανομής των ηλεκτρονίων μεταξύ ατόμων θείου και φθορίου, οδηγώντας στο σχηματισμό πολικών ομοιοπολικών δεσμών.