Διαφορά μεταξύ Achiral και Meso
Κύρια διαφορά – Achiral εναντίον Meso
Η χειραλικότητα είναι μια έννοια που εξηγεί τη διαφορά μεταξύ μορίων που έχουν τον ίδιο χημικό τύπο και μοριακό τύπο αλλά διαφέρουν μεταξύ τους. Αυτή η διαφορά προκύπτει λόγω της παρουσίας χειρόμορφων κέντρων. Ένα χειρόμορφο κέντρο είναι ένα άτομο άνθρακα που έχει τέσσερις διαφορετικούς υποκαταστάτες συνδεδεμένους σε αυτό. Τα μόρια που έχουν χειραλικότητα ονομάζονται χειρόμορφα μόρια. Αλλά δεν παρουσιάζουν όλα τα μόρια χειρικότητα. Υπάρχουν μερικά μόρια που δεν παρουσιάζουν χειρικότητα. Αυτά ονομάζονται μη χειρόμορφα μόρια. Υπάρχει επίσης μια άλλη ομάδα μορίων που έχει χειρόμορφα κέντρα αλλά είναι μη χειρόμορφα μόρια. Ονομάζονται μεσοενώσεις. Η κύρια διαφορά μεταξύ των δύο όρων μη χειρόμορφη και μεσο είναι ότι οι αχειρόμορφες ενώσεις δεν έχουν χειρόμορφα κέντρα ενώ οι μεσοενώσεις είναι ενδιάμεσες σε χειρόμορφες και μη χειρόμορφες ενώσεις.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το Achiral
– Ορισμός, εξήγηση της δομής με παραδείγματα
2. Τι είναι το Meso
– Ορισμός, Επεξήγηση της Δομής με Παραδείγματα, Τρόπος Αναγνώρισης
3. Ποιες είναι οι ομοιότητες μεταξύ Achiral και Meso
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ Achiral και Meso
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Achiral, Chemical Formula, Chiral, Chiral Center, Chirality, Inversion Center, Meso, Mirror Image, Molecular Formula
Τι είναι το Achiral
Ο όρος αχειρικό υποδηλώνει ότι δεν υπάρχουν χειρόμορφα κέντρα. Ένα χειρόμορφο κέντρο είναι ένα άτομο άνθρακα που έχει τέσσερις διαφορετικές ομάδες συνδεδεμένες σε αυτό. Δεδομένου ότι αυτές οι συνδεδεμένες ομάδες είναι διαφορετικές μεταξύ τους, η κατοπτρική εικόνα αυτού του χειρόμορφου κέντρου δεν μπορεί να υπερτεθεί μαζί του. Αλλά στις μη χειρόμορφες ενώσεις, δεν υπάρχουν χειρόμορφα κέντρα. Ως εκ τούτου, οι κατοπτρικές τους εικόνες είναι υπερτιθέμενες μεταξύ τους.
Οι αχειρόμορφες ενώσεις έχουν επίπεδο συμμετρίας. Αυτό σημαίνει ότι η διάταξη ενός μη χειρόμορφου μορίου σε ένα συγκεκριμένο επίπεδο μπορεί να χωριστεί σε δύο ίδια μισά. Όταν ένα μη χειρόμορφο μόριο διαιρείται με ένα υποθετικό επίπεδο, τα δύο μισά μοιάζουν με καθρέφτες το ένα του άλλου που μπορούν να τοποθετηθούν το ένα πάνω στο άλλο. Το ένα μισό του μορίου είναι η ακριβής αντανάκλαση του άλλου μισού.
Ο όρος κέντρο αναστροφής περιγράφει ένα σημείο σε ένα μόριο μέσω του οποίου όλα τα άτομα της αριστερής πλευράς μπορούν να ανακληθούν στο 180 για να ληφθεί το άλλο μισό αυτού του μορίου. Με άλλα λόγια, αν το ένα μισό από το σημείο αναστροφής περιστραφεί κατά 180, δίνει μια ίδια διάταξη με αυτή του άλλου μισού του μορίου. Επιπλέον, εάν ένα συγκεκριμένο μόριο έχει ένα άτομο άνθρακα στο κέντρο συνδεδεμένο σε τέσσερις πλευρικές ομάδες, αλλά αυτές οι πλευρικές ομάδες είναι πανομοιότυπες μεταξύ τους, τότε είναι μη χειρόμορφο μόριο.
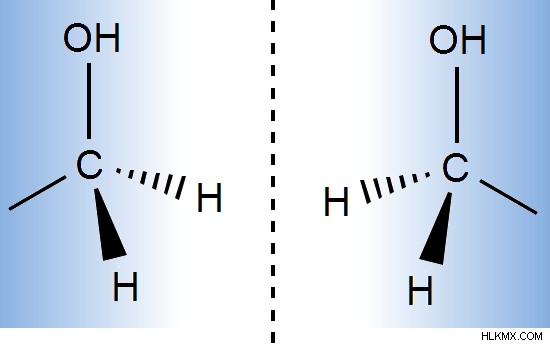
Εικόνα 1:Η μεθανόλη έχει μια υπερτιθέμενη εικόνα καθρέφτη
Το παραπάνω μόριο έχει τρία πανομοιότυπα άτομα συνδεδεμένα με το κεντρικό άτομο άνθρακα. Επομένως, το μόριο είναι μη χειρόμορφο.
Χαρακτηριστικά μιας αχειρικής ένωσης
Για να κατηγοριοποιηθεί ως μη χειρόμορφη ένωση, ένα μόριο θα πρέπει να έχει:
- Τουλάχιστον ένα επίπεδο συμμετρίας.
- Ένα σημείο αναστροφής.
- Λιγότερος αριθμός ατόμων ή ομάδων ατόμων (λιγότερα από τέσσερα) που συνδέονται με το άτομο άνθρακα (οι ενώσεις που έχουν διπλούς ή τριπλούς δεσμούς είναι μη χειρόμορφες).
Εάν ένα συγκεκριμένο μόριο έχει τουλάχιστον μία από τις παραπάνω ιδιότητες, τότε είναι μη χειρόμορφο μόριο.
Τι είναι το Meso
Μια μεσο ένωση αποτελείται από πολλαπλά χειρόμορφα κέντρα, αλλά έχει μια υπερτιθέμενη κατοπτρική εικόνα. Επομένως, μια μεσο ένωση εμφανίζει ιδιότητες που είναι ενδιάμεσες σε χειρόμορφες και μη χειρόμορφες ενώσεις. Αυτό σημαίνει ότι οι μεσοενώσεις έχουν δύο ή περισσότερα χειρόμορφα κέντρα όπως οι χειρόμορφες ενώσεις, αλλά η κατοπτρική εικόνα της μεσοένωσης μπορεί να υπερτεθεί με το μόριο, όπως τα μη χειρόμορφα μόρια.
Αν και υπάρχουν χειρόμορφα κέντρα σε μεσο ενώσεις, αυτά είναι οπτικά ανενεργά. Γενικά, μια μεσο ένωση έχει δύο ή περισσότερα χειρόμορφα κέντρα. Αλλά υπάρχει ένα επίπεδο που μπορεί να διαιρέσει το μόριο για να δώσει δύο ίδια μισά. Επειδή υπάρχουν πανομοιότυπα μισά, το μόριο είναι οπτικά ανενεργό.
Πώς να αναγνωρίσετε μια ένωση Meso
Οι παρακάτω συμβουλές μπορεί να είναι χρήσιμες για τον προσδιορισμό μιας μεσοένωσης.
- Η ένωση θα πρέπει να έχει δύο ή περισσότερα χειρόμορφα κέντρα.
- Η ένωση θα πρέπει να έχει ένα συμμετρικό επίπεδο που μπορεί να δώσει δύο ίδια μισά του μορίου.
- Η περιστροφή του μορίου κατά τη φορά των δεικτών του ρολογιού (R) θα πρέπει να δίνει τον ίδιο μοριακό τύπο σαν να περιστρέφονταν το μόριο προς την αριστερόστροφη φορά (S).
Η ένωση Ameso πρέπει να έχει ένα συμμετρικό επίπεδο μαζί με τα χειρόμορφα κέντρα. Εάν το μόριο περιστρέφεται δεξιόστροφα, θα πρέπει να δώσει τη διάταξη των ατόμων που δίνει όταν το μόριο περιστρέφεται αριστερόστροφα. Με αυτόν τον τρόπο, η ισομέρεια R και S ακυρώνεται, καθιστώντας την ένωση οπτικά ανενεργή.
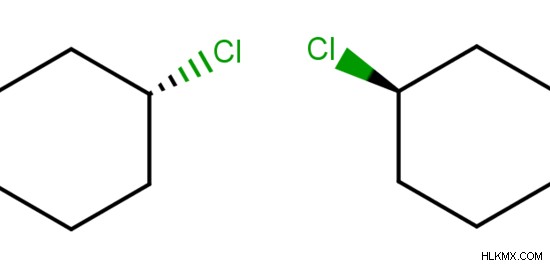
Εικόνα 2:Μια ένωση Meso
Η παραπάνω εικόνα δείχνει μια μεσοσύνθεση. Εδώ, η ένωση έχει δύο ασύμμετρα χειρόμορφα κέντρα. Αυτά είναι τα άτομα άνθρακα που συνδέονται με τα δύο άτομα χλωρίου. Υπάρχει ένα επίπεδο συμμετρίας. Το μισό του μορίου με το ένα άτομο χλωρίου υπερτίθεται με το άλλο μισό με το άλλο άτομο χλωρίου. Το πιο σημαντικό, η περιστροφή του μορίου δεξιόστροφα, δίνει τη διάταξη του μορίου που δίνεται όταν περιστρέφεται αριστερόστροφα.
Ομοιότητες μεταξύ Achiral και Meso
- Και οι δύο τύποι ενώσεων έχουν ένα επίπεδο συμμετρίας.
- Και οι δύο ενώσεις έχουν υπερτιθέμενες κατοπτρικές εικόνες.
Διαφορά μεταξύ Achiral και Meso
Ορισμός
Achiral: Η αχειρική ένωση δεν έχει χειρόμορφα κέντρα και έχει μια υπερτιθέμενη κατοπτρική εικόνα.
Μέσο: Μια μεσο ένωση αποτελείται από πολλαπλά χειρόμορφα κέντρα, αλλά έχει μια υπερτιθέμενη κατοπτρική εικόνα.
Παρουσία Chiral Centers
Achiral: Δεν υπάρχουν χειρόμορφα κέντρα σε μη χειρόμορφες ενώσεις.
Μέσο: Υπάρχουν πολλά χειρόμορφα κέντρα σε μεσοενώσεις.
Κέντρο αντιστροφής
Achiral: Οι αχειρόμορφες ενώσεις μπορούν να έχουν κέντρα αναστροφής.
Μέσο: Οι ενώσεις Meso δεν έχουν κέντρα αναστροφής.
Συμπέρασμα
Οι αχειρόμορφες ενώσεις και οι μεσοενώσεις σχετίζονται μεταξύ τους σε ορισμένες ιδιότητες, αλλά έχουν και κάποιες διαφορετικές ιδιότητες. Η κύρια διαφορά μεταξύ μη χειρόμορφων και μεσόμορφων ενώσεων είναι ότι οι μη χειρόμορφες ενώσεις δεν έχουν χειρόμορφα κέντρα, ενώ οι μεσο ενώσεις είναι ενδιάμεσες σε χειρόμορφες και μη χειρόμορφες ενώσεις.