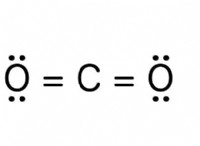Τι είναι ο ομοιοπολικός δεσμός αν τα άτομα μοιράζονται εξίσου εκλογικά;
Εδώ είναι γιατί:
* πολικότητα: Η πολικότητα σε έναν δεσμό αναφέρεται στην ανομοιογενή κατανομή της πυκνότητας ηλεκτρονίων. Εάν τα ηλεκτρόνια μοιράζονται εξίσου, δεν υπάρχει "πόλος" μεγαλύτερης πυκνότητας ηλεκτρονίων, καθιστώντας τον δεσμό μη πολικό.
* Ηλεκτροργατιστικότητα: Η διαφορά στην ηλεκτροαρνητικότητα μεταξύ δύο ατόμων καθορίζει πόσο εξίσου μοιράζονται ηλεκτρόνια. Όταν η διαφορά ηλεκτροαρνητικότητας είναι μικρή (συνήθως μικρότερη από 0,5), ο δεσμός θεωρείται μη πολικός.
* Συμμετρία: Οι μη πολικοί ομοιοπολικοί δεσμοί εμφανίζονται συχνά μεταξύ πανομοιότυπων ατόμων (όπως Η-Η σε αέριο υδρογόνου) ή όταν το μόριο έχει συμμετρική δομή, οδηγώντας σε ισορροπημένη κατανομή της πυκνότητας ηλεκτρονίων.
Παραδείγματα μη πολικών ομοιοπολικών δεσμών:
* H₂ (αέριο υδρογόνου)
* CL₂ (αέριο χλωρίου)
* O₂ (αέριο οξυγόνου)
* Ch₄ (μεθάνιο)
Σημαντική σημείωση: Ακόμη και σε μόρια με μη πολικούς δεσμούς, ολόκληρο το μόριο μπορεί ακόμα να είναι πολικό εάν η γεωμετρία του οδηγεί σε ανομοιογενή κατανομή της φορτίου.