Ποια είναι η φόρτιση σε ένα άτομο οξυγόνου;
Εδώ είναι γιατί:
* Ατομική δομή: Το οξυγόνο έχει 8 πρωτόνια (θετικά φορτισμένα) και 8 ηλεκτρόνια (αρνητικά φορτισμένα) στην ουδέτερη κατάσταση του.
* ίσες χρεώσεις: Οι θετικές και αρνητικές χρεώσεις εξισορροπούν ο ένας τον άλλον, με αποτέλεσμα ένα ουδέτερο άτομο.
Ωστόσο, το οξυγόνο συχνά σχηματίζει ιόντα κερδίζοντας ή απώλεια ηλεκτρονίων. Σε αυτή την περίπτωση, μπορεί να έχει χρέωση:
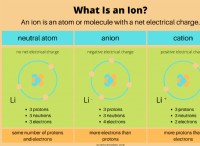
* ανιόν οξυγόνου (o²⁻): Το οξυγόνο μπορεί να κερδίσει δύο ηλεκτρόνια για να επιτύχει μια σταθερή ρύθμιση οκτάδων, με αποτέλεσμα μια φόρτιση -2.
* κατιόν οξυγόνου (o⁺): Ενώ είναι λιγότερο κοινό, το οξυγόνο μπορεί να χάσει ηλεκτρόνια για να σχηματίσει ένα κατιόν με θετικό φορτίο.
Έτσι, είναι σημαντικό να εξετάσουμε το πλαίσιο όταν μιλάμε για την φόρτιση ενός ατόμου οξυγόνου. Στη στοιχειακή του μορφή, είναι ουδέτερη. Αλλά σε ενώσεις ή όταν σχηματίζει ιόντα, μπορεί να έχει χρέωση.