Μια ουσία ή ένα μόριο που περιέχει δεσμούς άνθρακα άνθρακα άνθρακα-υδρογόνου;
Εδώ είναι γιατί:
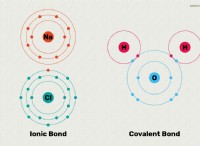
* Η ικανότητα συγκόλλησης του άνθρακα: Ο άνθρακας έχει τη μοναδική ικανότητα να σχηματίζει τέσσερις ομοιοπολικούς δεσμούς με άλλα άτομα, συμπεριλαμβανομένου του ίδιου. Αυτό επιτρέπει τον σχηματισμό μακρών αλυσίδων, διακλαδισμένων δομών και δαχτυλιδιών ατόμων άνθρακα.
* Ο ρόλος του υδρογόνου: Το υδρογόνο σχηματίζει εύκολα δεσμούς με άνθρακα, συμβάλλοντας στην ποικιλομορφία και την πολυπλοκότητα των οργανικών ενώσεων.
Βασικά χαρακτηριστικά των οργανικών ενώσεων:
* Αποτελούνται κυρίως από άνθρακα και υδρογόνο, αλλά συχνά περιέχουν άλλα στοιχεία όπως το οξυγόνο, το άζωτο, το θείο, ο φωσφόρος και τα αλογόνα.
* Παρουσιάζουν μια τεράστια ποικιλία δομών, ιδιοτήτων και λειτουργιών.
* Είναι ζωτικής σημασίας για τη ζωή και αποτελούν τη βάση πολλών βασικών μορίων όπως υδατάνθρακες, πρωτεΐνες, λιπίδια και νουκλεϊνικά οξέα.
Παραδείγματα οργανικών ενώσεων:
* μεθάνιο (CH4): Μια απλή οργανική ένωση με τέσσερις δεσμούς άνθρακα-υδρογόνου.
* αιθανόλη (C2H5OH): Ένα κοινό αλκοόλ με δεσμό άνθρακα-άνθρακα και αρκετούς δεσμούς άνθρακα-υδρογόνου.
* γλυκόζη (C6H12O6): Μια απλή ζάχαρη που είναι ένα θεμελιώδες δομικό στοιχείο υδατανθράκων.
* DNA και RNA: Σύνθετα οργανικά μόρια που περιέχουν μεγάλες αλυσίδες νουκλεοτιδίων που περιέχουν άνθρακα που φέρουν γενετικές πληροφορίες.
Εξαιρέσεις:
Υπάρχουν μερικές εξαιρέσεις στον κανόνα. Ορισμένες ενώσεις, όπως το διοξείδιο του άνθρακα (CO2), το μονοξείδιο του άνθρακα (CO) και τα ανθρακικά, περιέχουν άνθρακα αλλά δεν έχουν δεσμούς άνθρακα-υδρογόνου και συνεπώς δεν θεωρούνται οργανικοί.