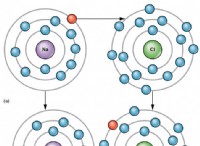
Γιατί τα άτομα σχηματίζουν ένωση αντί να υπάρχουν ως μεμονωμένα άτομα;
Εδώ είναι μια κατανομή:
* Κανόνας οκτάδων: Τα περισσότερα άτομα είναι πιο σταθερά όταν έχουν οκτώ ηλεκτρόνια στο εξωτερικό επίπεδο ενέργειας τους (κέλυφος σθένους). Αυτό είναι γνωστό ως κανόνας οκτάδων. Οι εξαιρέσεις περιλαμβάνουν υδρογόνο και ήλιο, τα οποία είναι σταθερά με δύο ηλεκτρόνια.
* Ηλεκτροργατιστικότητα: Τα άτομα έχουν ποικίλους βαθμούς έλξης για ηλεκτρόνια. Αυτή η έλξη ονομάζεται ηλεκτροαρνητικότητα.
* Τύποι σύνδεσης:
* Ιονική σύνδεση: Όταν τα άτομα έχουν μεγάλη διαφορά ηλεκτροαρνητικότητας, ένα άτομο μπορεί να μεταφέρει πλήρως ένα ηλεκτρόνιο σε άλλο άτομο, σχηματίζοντας ιόντα με αντίθετες χρεώσεις. Αυτές οι αντίθετες χρεώσεις προσελκύουν και δημιουργούν ένα ιοντικό δεσμό.
* ομοιοπολική σύνδεση: Όταν τα άτομα έχουν παρόμοια ηλεκτροαρνητικότητα, μοιράζονται ηλεκτρόνια για να επιτύχουν τον κανόνα οκτάδων. Αυτή η κατανομή των ηλεκτρονίων έχει ως αποτέλεσμα έναν ομοιοπολικό δεσμό.
* Μεταλλική σύνδεση: Στα μέταλλα, τα ηλεκτρόνια απομακρύνονται σε ολόκληρη τη δομή, με αποτέλεσμα μια ισχυρή έλξη μεταξύ των μεταλλικών ιόντων και της θάλασσας των ηλεκτρονίων.
Γιατί να σχηματίσουν ενώσεις;
* σταθερότητα: Δημιουργώντας ομόλογα, τα άτομα επιτυγχάνουν μια πιο σταθερή διαμόρφωση ηλεκτρονίων, εκπληρώνοντας τον κανόνα οκτάδων και μειώνοντας την ενέργειά τους.
* Διαφορετικότητα: Η χημική σύνδεση επιτρέπει τη δημιουργία μιας τεράστιας σειράς ενώσεων με διαφορετικές ιδιότητες.
* Βιολογική σημασία: Οι ενώσεις είναι απαραίτητες για τη ζωή. Για παράδειγμα, το νερό (H₂O) είναι ένας κρίσιμος διαλύτης για βιολογικές διεργασίες και οι πρωτεΐνες είναι κατασκευασμένες από μακρές αλυσίδες αμινοξέων που συνδέονται με ομοιοπολικούς δεσμούς.
Γιατί να μην υπάρχουν ως μεμονωμένα άτομα;
* Εξαιρέσεις: Ορισμένα ευγενή αέρια, όπως το ήλιο (He) και το νέον (NE), έχουν ήδη ένα πλήρες εξωτερικό κέλυφος ηλεκτρονίων και υπάρχουν ως μεμονωμένα άτομα. Αυτά τα αέρια είναι πολύ αντιδραστικά επειδή είναι ήδη σταθερά.
* Ενέργεια: Τα περισσότερα άτομα είναι πιο ενεργά ευνοϊκά όταν είναι συνδεδεμένα μαζί. Γι 'αυτό τείνουν να σχηματίζουν ενώσεις.
Συνοπτικά, τα άτομα σχηματίζουν ενώσεις επειδή αναζητούν μια πιο σταθερή διαμόρφωση ηλεκτρονίων, η οποία έχει ως αποτέλεσμα χαμηλότερα επίπεδα ενέργειας και αυξημένη αντιδραστικότητα. Αυτή η σταθερότητα επιτυγχάνεται μέσω διαφορετικών τύπων χημικών δεσμών, οδηγώντας στον σχηματισμό μιας τεράστιας σειράς ενώσεων με μοναδικές ιδιότητες.