Ποια είναι η σειρά μιας αντίδρασης υδρόλυσης;
Κατανόηση της σειράς αντίδρασης:
* Τάξη αντίδρασης αναφέρεται στον τρόπο με τον οποίο ο ρυθμός χημικής αντίδρασης επηρεάζεται από τη συγκέντρωση των αντιδραστηρίων.
* Αντιδράσεις πρώτης τάξης εξαρτάται από τη συγκέντρωση ενός αντιδραστηρίου. Ο διπλασιασμός της συγκέντρωσης αυτού του αντιδραστηρίου διπλασιάζει τον ρυθμό αντίδρασης.
* αντιδράσεις δεύτερης τάξης εξαρτάται από τη συγκέντρωση δύο αντιδραστηρίων ή το τετράγωνο της συγκέντρωσης ενός αντιδραστηρίου. Ο διπλασιασμός της συγκέντρωσης είτε του αντιδραστηρίου θα τετραπλασιάσει τον ρυθμό αντίδρασης.
* αντιδράσεις μηδενικής τάξης είναι ανεξάρτητα από τη συγκέντρωση των αντιδραστηρίων.
Παραδείγματα υδρόλυσης:
* Η υδρόλυση των εστέρων είναι συνήθως δεύτερη σειρά. Αυτό περιλαμβάνει τον εστέρα και ένα μόριο νερού. Ο ρυθμός εξαρτάται από τις συγκεντρώσεις τόσο του εστέρα όσο και του νερού.
* Η υδρόλυση ορισμένων αμιδίων μπορεί να είναι πρώτη σειρά. Εάν η συγκέντρωση του νερού είναι πολύ υψηλή, γίνεται ουσιαστικά σταθερή. Σε αυτή την περίπτωση, ο ρυθμός εξαρτάται κυρίως από τη συγκέντρωση του αμιδίου.
* Η υδρόλυση μιας απλής ζάχαρης όπως η σακχαρόζη είναι μια αντίδραση ψευδο-πρώτης τάξης. Αυτό οφείλεται στο γεγονός ότι το νερό είναι υπερβολικό, καθιστώντας την συγκέντρωσή του αποτελεσματικά σταθερή.
Βασικοί παράγοντες που επηρεάζουν τη σειρά:
* Μηχανισμός: Ο ειδικός μηχανισμός της αντίδρασης υδρόλυσης υπαγορεύει το στάδιο καθορισμού του ρυθμού, το οποίο επηρεάζει τη σειρά.
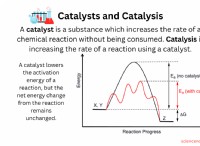
* Catalyst: Η παρουσία ενός καταλύτη μπορεί να μεταβάλει τον μηχανισμό και να αλλάξει τη σειρά αντίδρασης.
* ph: Η οξύτητα ή η αλκαλικότητα του διαλύματος μπορεί να επηρεάσει τον ρυθμό αντίδρασης και τη σειρά.
Συνοπτικά: Η σειρά αντίδρασης υδρόλυσης δεν είναι σταθερή τιμή. Εξαρτάται από τα συγκεκριμένα μόρια που εμπλέκονται, τις συνθήκες και τον μηχανισμό της αντίδρασης.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σε έναν συγκεκριμένο τύπο αντίδρασης υδρόλυσης.