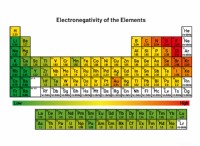
Το πυρίτιο και το χλώριο θα κάνουν μια ιοντική ένωση;
* Διαφορά ηλεκτροαρνητικότητας: Οι ιοντικοί δεσμοί σχηματίζονται όταν υπάρχει σημαντική διαφορά στην ηλεκτροαρνητικότητα μεταξύ δύο ατόμων. Το πυρίτιο (SI) έχει ηλεκτροαρνητικότητα 1,9, ενώ το χλώριο (CL) έχει ηλεκτροαρνητικότητα 3,16. Η διαφορά είναι 1,26, η οποία δεν είναι αρκετά μεγάλη για να σχηματίσει καθαρά ιοντικό δεσμό.
* ομοιοπολική σύνδεση: Η διαφορά ηλεκτροαρνητικότητας μεταξύ πυρίτιο και χλώριο υποδηλώνει ότι πιθανότατα θα σχηματίσουν έναν ομοιοπολικό δεσμό . Σε έναν ομοιοπολικό δεσμό, τα άτομα μοιράζονται ηλεκτρόνια και όχι ένα άτομο που μεταφέρει πλήρως ένα ηλεκτρόνιο στο άλλο.
* τετραχλωρίδιο πυριτίου (SICL4): Η ένωση που σχηματίζεται από πυρίτιο και χλώριο είναι τετραχλωρίδιο πυριτίου (SICL4). Πρόκειται για μια μοριακή ένωση με ομοιοπολικούς δεσμούς μεταξύ των ατόμων πυριτίου και χλωρίου.
Συνοπτικά: Ενώ η διαφορά ηλεκτροαρνητικότητας μεταξύ πυριτίου και χλωρίου υποδηλώνει κάποιο βαθμό ιοντικού χαρακτήρα, δεν είναι αρκετά μεγάλη για να σχηματίσει μια πραγματική ιοντική ένωση. Αντ 'αυτού, σχηματίζουν μια ομοιοπολική ένωση.