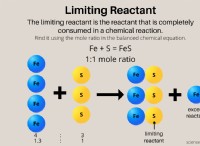
Περιγράψτε πώς οι ιδιότητες του σουλφιδίου σιδήρου είναι διαφορετικές από το θείο;
θείο:
* εμφάνιση: Κίτρινο, εύθραυστο στερεό.
* κατάσταση ύλης: Στερεό σε θερμοκρασία δωματίου.
* Σημείο τήξης: Χαμηλό σημείο τήξης (115,21 ° C).
* σημείο βρασμού: Χαμηλό σημείο βρασμού (444,6 ° C).
* Διαλυτότητα: Αδιάλυτο στο νερό.
* Αντιδραστικότητα: Αντιδρά με μέταλλα για να σχηματίσουν σουλφίδια, αλλά σχετικά μη αντιδραστικά με άλλα μη μέταλλα.
* Μαγνητικές ιδιότητες: Μη μαγνητική.
* αγωγιμότητα: Κακός αγωγός ηλεκτρικής ενέργειας.
σουλφίδιο σιδήρου:
* εμφάνιση: Μαύρο ή σκούρο γκρι στερεό, συχνά με μεταλλική λάμψη.
* κατάσταση ύλης: Στερεό σε θερμοκρασία δωματίου.
* Σημείο τήξης: Υψηλότερο σημείο τήξης από το θείο (1193 ° C).
* σημείο βρασμού: Υψηλότερο σημείο βρασμού από το θείο (2148 ° C).
* Διαλυτότητα: Αδιάλυτο στο νερό.
* Αντιδραστικότητα: Αντιδρά με οξέα για την παραγωγή αερίου υδρογόνου.
* Μαγνητικές ιδιότητες: Ασθενώς μαγνητικό λόγω της παρουσίας σιδήρου.
* αγωγιμότητα: Ελαφρώς καλύτερος αγωγός ηλεκτρικής ενέργειας από το θείο.
Βασικές διαφορές:
* Χρώμα και εμφάνιση: Το θείο είναι κίτρινο ενώ το σουλφίδιο του σιδήρου είναι μαύρο/γκρι.
* Σημείο τήξης και βρασμού: Το σουλφίδιο του σιδήρου έχει σημαντικά υψηλότερα σημεία τήξης και βρασμού λόγω ισχυρότερων ιοντικών δεσμών.
* Αντιδραστικότητα: Το σουλφίδιο του σιδήρου είναι πιο αντιδραστικό από το θείο.
* Μαγνητικές ιδιότητες: Το σουλφίδιο του σιδήρου είναι ασθενώς μαγνητικό ενώ το θείο δεν είναι.
* αγωγιμότητα: Το σουλφίδιο του σιδήρου είναι ένας ελαφρώς καλύτερος αγωγός ηλεκτρικής ενέργειας από το θείο.
Συνοπτικά: Το σουλφίδιο του σιδήρου είναι μια ένωση που σχηματίζεται από την αντίδραση του σιδήρου και του θείου, οδηγώντας σε μια νέα ουσία με πολύ διαφορετικές ιδιότητες σε σύγκριση με το καθαρό θείο.