Ποια είναι η ισορροπημένη εξίσωση για το νιτρικό οξύ και το υδρογενικό νάτριο;
hno₃ (aq) + nahco₃ (aq) → nano₃ (aq) + h₂o (l) + co₂ (g)
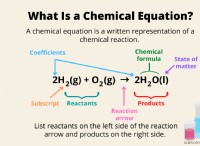
Ακολουθεί μια ανάλυση της αντίδρασης:
* Αντιδραστήρια:
* Το νιτρικό οξύ (HNO₃) είναι ένα ισχυρό οξύ.
* Το υδρογενικό νάτριο (NAHCO₃), επίσης γνωστό ως σόδα ψησίματος, είναι μια βάση.
* Προϊόντα:
* Το νιτρικό νάτριο (Nano₃) είναι ένα διαλυτό αλάτι.
* Το νερό (H₂O) σχηματίζεται ως υγρό.
* Το διοξείδιο του άνθρακα (CO₂) απελευθερώνεται ως αέριο, συχνά προκαλεί αναστάτωση ή φυσαλίδες.
Αυτή η αντίδραση είναι ένα κλασικό παράδειγμα μιας αντίδρασης εξουδετέρωσης οξέος βάσης, όπου ένα οξύ και μια βάση αντιδρούν για να σχηματίσουν ένα άλας και νερό. Το αέριο διοξειδίου του άνθρακα είναι ένα μοναδικό υποπροϊόν αυτής της συγκεκριμένης αντίδρασης.