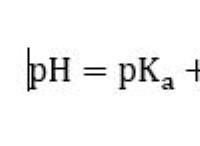Το ανθρακικό νάτριο έχει πολικό ομοιοπολικό δεσμό με νερό;
* Ιονική φύση του ανθρακικού νατρίου: Το ανθρακικό νάτριο είναι μια ιοντική ένωση. Αποτελείται από ιόντα νατρίου (Na⁺) και ιόντα ανθρακικού άλατος (Co₃2⁻) που συγκρατούνται από ηλεκτροστατικές δυνάμεις.
* Πόλη του νερού: Το νερό (H₂O) είναι ένα πολικό μόριο λόγω της διαφοράς ηλεκτροαρνητικότητας μεταξύ των ατόμων οξυγόνου και υδρογόνου, δημιουργώντας ένα μερικό αρνητικό φορτίο στο οξυγόνο και μερικές θετικές φορτίσεις στα υδρογόνα.
* αλληλεπίδραση: Όταν το ανθρακικό νάτριο διαλύεται σε νερό, υφίσταται ιονικές αλληλεπιδράσεις . Τα πολικά μόρια νερού περιβάλλουν τα ιόντα, τα προσελκύουν και τα τραβώντας τους. Τα θετικά ιόντα νατρίου προσελκύονται από το αρνητικό άκρο του οξυγόνου των μορίων νερού, ενώ τα αρνητικά ιόντα ανθρακικού άλατος προσελκύονται από τα θετικά άκρα υδρογόνου των μορίων νερού.
Επομένως, η αλληλεπίδραση μεταξύ ανθρακικού νατρίου και νερού είναι μια ιοντική αλληλεπίδραση, όχι ένας πολικός ομοιοπολικός δεσμός.