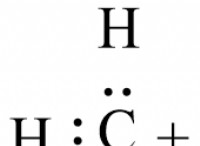Ποια είναι η μάζα του αζώτου που μπορεί να παρασχεθεί με χλωριούχο αμμώνιο 5,0 kg;
1. Προσδιορίστε τη μοριακή μάζα χλωριούχου αμμωνίου και αζώτου:
* nh₄cl: (14,01 g/mol n) + (4 * 1,01 g/mol h) + (35,45 g/mol cl) =53,49 g/mol
* n₂: 2 * (14,01 g/mol n) =28,02 g/mol
2. Υπολογίστε τις γραμμομορείς χλωριούχου αμμωνίου:
* Μετατρέψτε τη μάζα χλωριούχου αμμωνίου σε γραμμάρια:5,0 kg * 1000 g/kg =5000 g
* Διαχωρίστε τη μάζα με τη μοριακή μάζα:5000 g / 53,49 g / mol =93,4 mol NH₄CL
3. Προσδιορίστε την αναλογία mole του αζώτου προς το χλωριούχο αμμώνιο:
* Ο χημικός τύπος NH₄CL δείχνει ότι υπάρχει 1 μοσχάρι αζώτου (Ν) για κάθε 1 γραμμομόριο χλωριούχου αμμωνίου (NH₄Cl).
4. Υπολογίστε τα μολυσματικά του αζώτου:
* Δεδομένου ότι η αναλογία mole είναι 1:1, οι γραμμομορείς του αζώτου είναι ίσες με τις γραμμομόρια χλωριούχου αμμωνίου:93,4 mol n
5. Υπολογίστε τη μάζα του αζώτου:
* Πολλαπλασιάστε τις γραμμομορίες του αζώτου με τη μοριακή μάζα του αζώτου:93,4 mol * 28,02 g/mol =2618 g
6. Μετατρέψτε τη μάζα του αζώτου σε κιλά:
* Διαχωρίστε τη μάζα κατά 1000:2618 g / 1000 g / kg =2,618 kg
Επομένως, 5,0 kg χλωριούχου αμμωνίου μπορεί να παρέχει περίπου 2,618 kg αζώτου.