Ποιος είναι ο διαχωρισμός των φορτίων μέσα σε ένα πολικό μόριο που ονομάζεται;
Εδώ είναι γιατί:
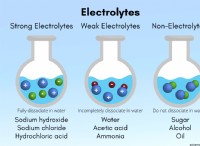
* πολικά μόρια: Αυτά τα μόρια έχουν ανομοιογενή κατανομή ηλεκτρονίων, οδηγώντας σε ένα ελαφρώς θετικό τέλος και ένα ελαφρώς αρνητικό τέλος.
* Διπολική στιγμή: Αυτό είναι ένα μέτρο του διαχωρισμού αυτών των θετικών και αρνητικών χρεώσεων. Αντιπροσωπεύεται από ένα διάνυσμα που δείχνει από το θετικό έως το αρνητικό άκρο του μορίου.
Σκεφτείτε το σαν ένα μικροσκοπικό μαγνήτη μέσα στο μόριο, με βόρειο και νότιο πόλο.