Ποιοι τύποι ατόμων σχηματίζονται από την ομοιοπολική συγκόλληση;
Εδώ είναι γιατί:
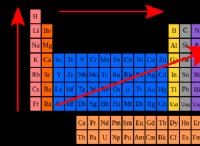
* Μη μέταλλα Έχετε υψηλή ηλεκτροαρνητικότητα, που σημαίνει ότι προσελκύουν έντονα ηλεκτρόνια.
* Σε ομοιοπολική συγκόλληση, τα άτομα μοιράζονται ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων (συνήθως ένα οκτάτο, όπως τα ευγενή αέρια). Αυτή η κοινή χρήση συμβαίνει επειδή ούτε το άτομο δεν μπορεί εύκολα να κερδίσει ή να χάσει ηλεκτρόνια για να γίνει ιόν.
Παραδείγματα ομοιοπολικής σύνδεσης:
* νερό (h₂o): Το υδρογόνο (μη μέταλλο) και το οξυγόνο (μη μεταλλικό) μοιράζονται ηλεκτρόνια.
* διοξείδιο του άνθρακα (CO₂): Ο άνθρακας (μη μέταλλο) και το οξυγόνο (μη μέταλλο) μοιράζονται ηλεκτρόνια.
* μεθάνιο (ch₄): Ο άνθρακας (μη μέταλλο) και το υδρογόνο (μη μέταλλο) μοιράζονται ηλεκτρόνια.
* Αέριο αζώτου (n₂): Δύο άτομα αζώτου (μη μέταλλα) μοιράζονται ηλεκτρόνια.
Εξαιρέσεις:
Υπάρχουν μερικές εξαιρέσεις όπου ένα μέταλλο μπορεί να σχηματίσει έναν ομοιοπολικό δεσμό με μη μέταλλο, αλλά αυτό είναι λιγότερο συνηθισμένο.