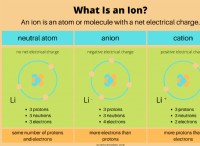
Ποιος είναι ο διαχωρισμός μιας ένωσης στα συστατικά της ιόντα;
διάσταση είναι μια διαδικασία όπου μια ένωση διασπάται στα μεμονωμένα ιόντα της όταν διαλύεται σε ένα διαλύτη, συνήθως νερό. Αυτό συμβαίνει όταν οι ιοντικές ενώσεις, οι οποίες συγκρατούνται από ηλεκτροστατικά αξιοθέατα μεταξύ των αντιθέτων ιόντων, αλληλεπιδρούν με τα πολικά μόρια νερού.
Ακολουθεί μια ανάλυση της διαδικασίας:
* Ιονική ένωση: Αυτές οι ενώσεις σχηματίζονται από την ηλεκτροστατική έλξη μεταξύ θετικά φορτισμένων κατιόντων και αρνητικά φορτισμένων ανιόντων.
* Διαλύτης (συνήθως νερό): Τα μόρια του νερού είναι πολικά, που σημαίνει ότι έχουν ένα ελαφρώς θετικό και ελαφρώς αρνητικό άκρο λόγω της ανομοιογενούς κατανομής των ηλεκτρονίων.
* αλληλεπίδραση: Το θετικό τέλος των μορίων του νερού προσελκύει τα αρνητικά φορτισμένα ανιόντα, ενώ το αρνητικό τέλος των μορίων του νερού προσελκύει τα θετικά φορτισμένα κατιόντα.
* Διάσπαση: Αυτή η αλληλεπίδραση αποδυναμώνει τις ηλεκτροστατικές δυνάμεις που συγκρατούν τα ιόντα μαζί στην ένωση, προκαλώντας τη διάσπαση της ένωσης στα μεμονωμένα ιόντα της.
Παράδειγμα:
Όταν το αλάτι του τραπεζιού (NaCl) διαλύεται στο νερό, διαχωρίζεται σε ιόντα νατρίου (Na+) και σε ιόντα χλωριούχου (Cl-):
NaCl (s) → Na + (aq) + cl- (aq)
Οπου:
* (ες) υποδεικνύει την στερεά κατάσταση
* (aq) υποδεικνύει ότι τα ιόντα διαλύονται στο νερό
Βασικά σημεία:
* Η διάσταση είναι μια αναστρέψιμη διαδικασία.
* Η έκταση της διάστασης εξαρτάται από την ένωση και τον διαλύτη.
* Η διάσταση διαδραματίζει κρίσιμο ρόλο σε πολλές χημικές και βιολογικές διεργασίες, όπως:
* Λύσεις ηλεκτρολύτη
* Αντιδράσεις οξέος-βάσης
* Βιολογικές διεργασίες που περιλαμβάνουν ιόντα (π.χ., νευρικές παρορμήσεις)