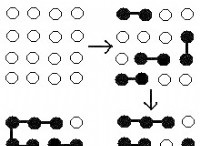
Γιατί οι ιοντικές ενώσεις είναι τόσο εύθραυστες;
* Κρυσταλλική δομή: Οι ιοντικές ενώσεις σχηματίζουν μια δομή πλέγματος όπου τα θετικά και τα αρνητικά ιόντα είναι διατεταγμένα σε ένα κανονικό, επαναλαμβανόμενο μοτίβο. Αυτή η δομή είναι πολύ άκαμπτη και άκαμπτη.
* ηλεκτροστατικές δυνάμεις: Τα ιόντα στο πλέγμα συγκρατούνται από ισχυρά ηλεκτροστατικά αξιοθέατα. Αυτές οι δυνάμεις είναι κατευθυντικές, που σημαίνει ότι ενεργούν κατά μήκος συγκεκριμένων γραμμών μεταξύ των ιόντων.
* Αντίκτυπος και μετατόπιση: Όταν ένας ιοντικός κρύσταλλος υποβάλλεται σε δύναμη, όπως ένα χτύπημα ή πίεση, τα ιόντα εκτοπίζονται από τις θέσεις τους. Αυτή η μετατόπιση διαταράσσει τα ηλεκτροστατικά αξιοθέατα που συγκρατούν τον κρύσταλλο.
* Απομάκρυνση και κάταγμα: Καθώς τα ιόντα μετατοπίζονται, οι χρεώσεις τους ευθυγραμμίζονται, έτσι ώστε όπως οι χρεώσεις (θετικές θετικές ή αρνητικές αρνητικές) έρχονται σε στενή εγγύτητα. Αυτά τα ιόντα απωθούν έντονα ο ένας τον άλλον, οδηγώντας σε ξαφνικό κάταγμα ή σπάσιμο του κρυστάλλου.
Αντίθετα, οι μεταλλικές ενώσεις είναι εύπλαστες και όλκιμοι επειδή τα ηλεκτρόνια τους είναι ελεύθερα να κινούνται, επιτρέποντας στα μεταλλικά ιόντα να γλιστρούν ο ένας τον άλλον χωρίς να διαταράσσουν τους μεταλλικούς δεσμούς.
Συνοπτικά, η ευκαμψία των ιοντικών ενώσεων προκύπτει από τις ισχυρές ηλεκτροστατικές δυνάμεις, την άκαμπτη δομή του πλέγματος και τη διάσπαση αυτών των δυνάμεων όταν τα ιόντα εκτοπίζονται υπό τάση.