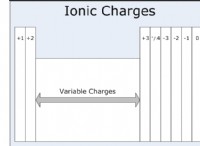
Πού βρίσκονται τα περισσότερα αντιδραστικά μέταλλα;
Εδώ είναι γιατί:
* Διαμόρφωση ηλεκτρονίων: Τα μέταλλα σε αυτές τις ομάδες έχουν μόνο ένα ή δύο ηλεκτρόνια σθένους (ηλεκτρόνια στο εξωτερικό κέλυφος). Αυτά τα ηλεκτρόνια είναι σχετικά χαλαρά συνδεδεμένα με το άτομο, καθιστώντας τα εύκολο να χάσουν και να σχηματίσουν θετικά ιόντα.
* Ηλεκτροποσωτικότητα: Αυτά τα μέταλλα έχουν μεγάλη τάση να χάσουν ηλεκτρόνια και να σχηματίζουν κατιόντα (θετικά φορτισμένα ιόντα). Αυτή η υψηλή ηλεκτροδιαστολή συμβάλλει στην αντιδραστικότητα τους.
Παραδείγματα:
* Ομάδα 1 (αλκαλικά μέταλλα): Το λίθιο (Li), το νάτριο (Na), το κάλιο (k), το ρουμπίντιο (RB), το καίσο (CS) και το francium (FR).
* Ομάδα 2 (αλκαλικά μέταλλα γης): Beryllium (ΒΕ), μαγνήσιο (mg), ασβέστιο (CA), στροντίου (SR), βάριο (BA) και ραδίου (RA).
Σημαντική σημείωση: Η αντιδραστικότητα αυξάνεται καθώς κατεβαίνετε αυτές τις ομάδες. Αυτό οφείλεται στο γεγονός ότι το εξώτατο ηλεκτρόνιο είναι πιο μακριά από τον πυρήνα και είναι λιγότερο σφιχτά.
Εξαιρέσεις:
Ενώ η ομάδα 1 και 2 μέταλλα είναι τα πιο αντιδραστικά, ορισμένα μέταλλα σε άλλες ομάδες μπορούν επίσης να είναι εξαιρετικά αντιδραστικά λόγω των μοναδικών ιδιοτήτων τους. Για παράδειγμα, το αλουμίνιο (AL) είναι αρκετά αντιδραστικό λόγω της τάσης του να σχηματίσει ένα προστατευτικό στρώμα οξειδίου.