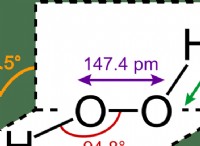
Τι συμβαίνει όταν το θείο αντιδρά με νιτρικό οξύ;
s + 6hno₃ → h₂so₄ + 6no₂ + 2h₂o
Ακολουθεί μια ανάλυση του τι συμβαίνει:
* θείο οξειδώνεται με νιτρικό οξύ, το οποίο δρα ως οξειδωτής.
* Νιτρικό οξύ (HNO₃) μειώνεται στο διοξείδιο του αζώτου (NO₂), το οποίο είναι ένα κόκκινο-καφέ αέριο.
* θειικό οξύ (h₂so₄) παράγεται ως το κύριο προϊόν.
* νερό (h₂o) παράγεται επίσης.
Οι συνθήκες αντίδρασης:
* Αυτή η αντίδραση είναι εξαιρετικά εξωθερμική (παράγει πολλή θερμότητα).
* Συνήθως πραγματοποιείται σε αυξημένες θερμοκρασίες .
* συμπυκνωμένο νιτρικό οξύ χρησιμοποιείται.
Τα προϊόντα:
* θειικό οξύ είναι ένα ισχυρό οξύ με ποικίλες βιομηχανικές χρήσεις.
* Διοξείδιο του αζώτου είναι ένα τοξικό και διαβρωτικό αέριο και είναι ένας σημαντικός ατμοσφαιρικός ρύπος.
Σημαντικές σημειώσεις:
* Αυτή η αντίδραση είναι μια πολύπλοκη διαδικασία με διάφορα βήματα. Η εξίσωση αντίδρασης που παρουσιάζεται παραπάνω είναι μια απλοποιημένη αναπαράσταση.
* Τα ακριβή προϊόντα και οι συνθήκες αντίδρασης μπορεί να διαφέρουν ανάλογα με τις συγκεκριμένες συνθήκες.
* Αυτή η αντίδραση χρησιμοποιείται στη βιομηχανική παραγωγή θειικού οξέος.
Αυτή η αντίδραση καταδεικνύει την οξειδωτική ισχύ του νιτρικού οξέος. Το νιτρικό οξύ χρησιμοποιείται συχνά ως ισχυρός οξειδωτικός παράγοντας σε διάφορες χημικές αντιδράσεις.