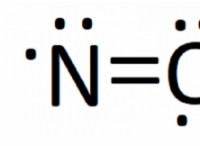Ποια ενεργειακή αλλαγή θα περιμένατε όταν ένα μόριο διαλύεται στα συστατικά του άτομα;
* Χημικοί δεσμοί αποθήκευσης ενέργειας: Ο σχηματισμός χημικών δεσμών μεταξύ των ατόμων απελευθερώνει ενέργεια, καθιστώντας το προκύπτον μόριο πιο σταθερό από τα ατομικά άτομα.
* Οι δεσμοί θραύσης απαιτούν ενέργεια: Για να σπάσετε αυτούς τους δεσμούς, πρέπει να τοποθετήσετε την ενέργεια πίσω στο σύστημα. Αυτό οφείλεται στο γεγονός ότι ξεπερνάτε τις ελκυστικές δυνάμεις που κρατούν τα άτομα μαζί.
Παράδειγμα:
Σκεφτείτε το μόριο νερού (H₂O). Οι δεσμοί υδρογόνου-οξυγόνου εντός της ενέργειας του νερού. Για να σπάσετε αυτούς τους δεσμούς και να διαχωρίσετε το μόριο σε μεμονωμένα άτομα υδρογόνου και οξυγόνου, πρέπει να παρέχετε ενέργεια, συνήθως με τη μορφή θερμότητας ή φωτός.
Βασικά σημεία:
* ενδοθερμική αντίδραση: Μια διαδικασία που απορροφά ενέργεια από το περιβάλλον της ονομάζεται ενδοθερμική αντίδραση. Το σπάσιμο ενός μορίου σε άτομα είναι μια ενδοθερμική διαδικασία.
* Ενθαλπία Bond: Η ποσότητα ενέργειας που απαιτείται για να σπάσει ένας συγκεκριμένος τύπος δεσμού ονομάζεται ενθαλπία δεσμού.
* Η αντίστροφη διαδικασία είναι εξωθερμική: Ο σχηματισμός ενός χημικού δεσμού από μεμονωμένα άτομα απελευθερώνει ενέργεια (εξωθερμική αντίδραση).
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σχετικά με οποιοδήποτε από αυτά τα σημεία!