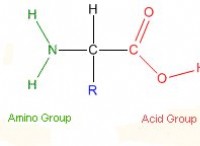
Τι σημαίνει διπλό ομοιοπολικό δεσμό;
* ομοιοπολικός δεσμός: Ένας ομοιοπολικός δεσμός εμφανίζεται όταν δύο άτομα μοιράζονται ηλεκτρόνια για να επιτευχθούν σταθερή διαμόρφωση ηλεκτρονίων (συνήθως ένα πλήρες εξωτερικό κέλυφος).
* Διπλός ομοιοπολικός δεσμός: Αυτός ο δεσμός περιλαμβάνει την ανταλλαγή * δύο * ζευγών ηλεκτρονίων, ή τέσσερα ηλεκτρόνια συνολικά, μεταξύ των δύο ατόμων.
Εδώ είναι μια οπτική αναπαράσταση:
`` `
O =o
`` `
Σε αυτό το παράδειγμα, τα άτομα οξυγόνου μοιράζονται δύο ζεύγη ηλεκτρονίων, σχηματίζοντας διπλό ομοιοπολικό δεσμό.
Χαρακτηριστικά διπλών δεσμών:
* Ισχυρότερο: Οι διπλοί δεσμοί είναι γενικά ισχυρότεροι από τους μεμονωμένους ομοιοπολικούς δεσμούς λόγω της αυξημένης κατανομής ηλεκτρονίων.
* Shorter: Οι διπλοί δεσμοί οδηγούν σε μικρότερες αποστάσεις μεταξύ των εμπλεκόμενων ατόμων.
* ακαμψία: Οι διπλοί δεσμοί προσδίδουν ακαμψία στα μόρια, επηρεάζοντας το σχήμα και την αντιδραστικότητα τους.
Παραδείγματα μορίων με διπλούς δεσμούς:
* οξυγόνο (o2): Το μόριο οξυγόνου έχει διπλό δεσμό.
* διοξείδιο του άνθρακα (CO2): Κάθε άτομο άνθρακα σε CO2 σχηματίζει διπλό δεσμό με κάθε άτομο οξυγόνου.
* αιθυλένιο (C2H4): Τα άτομα άνθρακα στο αιθυλένιο συνδέονται με διπλό δεσμό.
Επιτρέψτε μου να ξέρω αν θέλετε να εξερευνήσετε συγκεκριμένα παραδείγματα ή να έχετε περαιτέρω ερωτήσεις!