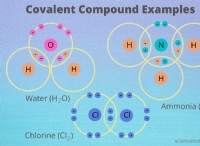
Ποιες είναι οι δείκτες που θα χρησιμοποιηθούν πιθανότατα εάν η ακόλουθη ουσία σχημάτισε ιοντικό δεσμό;
Κατανόηση ιοντικών δεσμών
* Ιονικά ομόλογα Η μορφή μεταξύ των μετάλλων (που τείνουν να χάνουν ηλεκτρόνια) και μη μέταλλα (τα οποία τείνουν να κερδίζουν ηλεκτρόνια).
* μέταλλα Γίνετε θετικά φορτισμένα ιόντα (κατιόντα).
* Μη μέταλλα γίνετε αρνητικά φορτισμένα ιόντα (Anions).
* Ο στόχος είναι να επιτευχθεί μια ουδέτερη ένωση, που σημαίνει ότι το συνολικό θετικό φορτίο πρέπει να ισούται με το συνολικό αρνητικό φορτίο.
Προσδιορισμός δεικτών
1. Προσδιορίστε τα στοιχεία: Πες μου τα στοιχεία που εμπλέκονται στον πιθανό ιοντικό δεσμό.
2. Προσδιορίστε τις χρεώσεις τους: Αναζητήστε τις τυπικές χρεώσεις αυτών των στοιχείων όταν σχηματίζουν ιόντα.
* μέταλλα: Συχνά έχουν ένα μόνο φορτίο (π.χ. νάτριο, Na+, μαγνήσιο, Mg2+)
* Μη μετάλλια: Μπορεί να έχει πολλαπλές χρεώσεις (π.χ. οξυγόνο, Ο2-, θείο, S2-, άζωτο, N3-)
3. Εξισορρόπηση των χρεώσεων: Βρείτε τη μικρότερη αναλογία ιόντων που θα κάνουν το συνολικό θετικό φορτίο ίσο με το συνολικό αρνητικό φορτίο.
Παράδειγμα
Ας πούμε ότι έχετε νάτριο (NA) και χλώριο (CL):
* Το νάτριο (Na) σχηματίζει ένα +1 ιόν (Na +)
* Το χλώριο (cl) σχηματίζει ένα -1 ιόν (cl-)
Δεδομένου ότι οι χρεώσεις είναι ήδη ίσες, ο τύπος θα ήταν naCl (δεν απαιτούνται δείκτες).
Πες μου τα εμπλεκόμενα στοιχεία και μπορώ να σας βοηθήσω να καταλάβετε τους δείκτες!