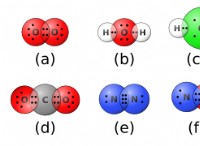
Η ιοντική δομή πλέγματος αποτελείται από ένα επαναλαμβανόμενο μοτίβο άτομα που συνδέονται με ομοιοπολικούς δεσμούς;
* Τα ιονικά πλέγματα συγκρατούνται από ηλεκτροστατικές δυνάμεις (ιοντικοί δεσμοί) όχι ομοιοπολικοί δεσμοί. Οι ομοιοπολικοί δεσμοί περιλαμβάνουν την κατανομή των ηλεκτρονίων μεταξύ των ατόμων, ενώ οι ιοντικοί δεσμοί περιλαμβάνουν τη μεταφορά ηλεκτρονίων από το ένα άτομο στο άλλο, δημιουργώντας θετικά και αρνητικά φορτισμένα ιόντα.
* Το επαναλαμβανόμενο πρότυπο των ιόντων είναι το καθοριστικό χαρακτηριστικό ενός ιοντικού πλέγματος. Τα θετικά και αρνητικά ιόντα οργανώνονται σε μια τρισδιάστατη δομή για να ελαχιστοποιήσουν την ηλεκτροστατική τους απόρριψη και να μεγιστοποιήσουν την έλξη.
Ακολουθεί μια κατανομή των βασικών σημείων:
* Ιωνικές ενώσεις: Σχηματίζεται από την ηλεκτροστατική έλξη μεταξύ των αντιθέτων ιόντων.
* Ιονικό πλέγμα: Η δομή 3D μιας ιοντικής ένωσης όπου τα ιόντα είναι διατεταγμένα σε ένα επαναλαμβανόμενο μοτίβο.
* Ιονικός δεσμός: Η ηλεκτροστατική έλξη μεταξύ των αντίθετα φορτισμένων ιόντων.
Παράδειγμα: Το χλωριούχο νάτριο (NaCl) σχηματίζει ένα ιοντικό πλέγμα. Τα άτομα νατρίου χάνουν ένα ηλεκτρόνιο για να γίνουν θετικά φορτισμένα ιόντα νατρίου (Na+), ενώ τα άτομα χλωρίου αποκτούν ένα ηλεκτρόνιο για να γίνουν αρνητικά φορτισμένα ιόντα χλωριούχου (Cl-). Αυτά τα ιόντα οργανώνονται σε ένα επαναλαμβανόμενο κυβικό μοτίβο λόγω της ηλεκτροστατικής έλξης μεταξύ τους.