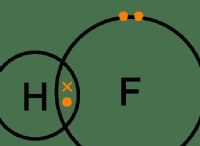
Τι είδους άτομα αποτελούν έναν ομοιοπολικό δεσμό;
* Κοινή χρήση ηλεκτρόνων: Οι ομοιοπολικοί δεσμοί περιλαμβάνουν την ανταλλαγή ηλεκτρονίων μεταξύ των ατόμων. Τα μη μέταλλα τείνουν να έχουν υψηλή ηλεκτροαρνητικότητα, που σημαίνει ότι έχουν ισχυρή έλξη για τα ηλεκτρόνια.
* Σταθερές διαμορφώσεις: Με την κοινή χρήση ηλεκτρονίων, τα μη μέταλλα άτομα μπορούν να επιτύχουν σταθερή διαμόρφωση ηλεκτρονίων, παρόμοια με εκείνη των ευγενών αερίων (τα οποία είναι πολύ αντιδραστικά).
Παραδείγματα ατόμων που αποτελούν ομοιοπολικά δεσμούς:
* υδρογόνο (h)
* οξυγόνο (o)
* άνθρακα (c)
* αζώτου (n)
* χλώριο (cl)
* Φθορίνη (F)
* φωσφόρος (p)
* θείο
Σημαντική σημείωση: Ενώ οι περισσότεροι ομοιοπολικοί δεσμοί σχηματίζονται μεταξύ των μη μεταλλικών, υπάρχουν εξαιρέσεις. Για παράδειγμα, ορισμένα μέταλλα μπορούν να σχηματίσουν ομοιοπολικούς δεσμούς με μη μέταλλα.