Διαφορά μεταξύ σαπωνοποίησης και εξουδετέρωσης
Κύρια διαφορά – Σαπωνοποίηση έναντι Εξουδετέρωσης
Η σαπωνοποίηση και η εξουδετέρωση είναι πολύ σημαντικές χημικές αντιδράσεις που χρησιμοποιούνται τόσο σε εργαστηριακή όσο και σε βιομηχανική κλίμακα. Η σαπωνοποίηση είναι γενικά ο σχηματισμός σαπουνιού με τη μορφή εναιωρήματος. Αυτό συμβαίνει λόγω της διάσπασης ενός τριγλυκεριδίου σε γλυκερίνη και λιπαρά οξέα. Εξουδετέρωση είναι ο σχηματισμός ενός ουδέτερου μέσου μετά από μια χημική αντίδραση. Αυτό μπορεί να παρατηρηθεί κυρίως σε αντιδράσεις οξέος-βάσης. Τα οξέα είναι ικανά να απελευθερώνουν ιόντα Η και οι βάσεις είναι ικανές να απελευθερώνουν ιόντα ΟΗ. Όταν όλα τα ιόντα Η που απελευθερώνονται από το οξύ αντιδρούν με όλα τα ιόντα ΟΗ που απελευθερώνονται από τη βάση, λέγεται ότι το μέσο έχει εξουδετερωθεί. Η κύρια διαφορά μεταξύ της σαπωνοποίησης και της εξουδετέρωσης είναι ότι η σαπωνοποίηση περιλαμβάνει τη διάσπαση ενός εστέρα σε αλκοόλη και καρβοξυλικό ιόν, ενώ η εξουδετέρωση περιλαμβάνει το σχηματισμό ενός ουδέτερου μέσου μετά τη χημική αντίδραση.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η σαπωνοποίηση
– Ορισμός, Μηχανισμός, Αλάτισμα
2. Τι είναι η Εξουδετέρωση
– Ορισμός, διαφορετικοί τύποι
3. Ποια είναι η διαφορά μεταξύ σαπωνοποίησης και εξουδετέρωσης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Βασικότητα, καρβοξυλικό οξύ, εστέρας, εξώθερμος, λιπαρά οξέα, γλυκερίνη, υδροξείδιο καλίου, σαπωνοποίηση, σαπούνι, τριγλυκερίδια

Τι είναι η σαπωνοποίηση
Η σαπωνοποίηση είναι μια διαδικασία κατά την οποία τα τριγλυκερίδια αντιδρούν με το υδροξείδιο του νατρίου ή του καλίου για να παράγουν γλυκερίνη και ένα άλας λιπαρού οξέος που ονομάζεται «σαπούνι». Η σαπωνοποίηση περιλαμβάνει τη διάσπαση ενός εστέρα σε καρβοξυλικό οξύ και αλκοόλη χρησιμοποιώντας NaOH ή ΚΟΗ παρουσία νερού. Εδώ, λόγω της βασικότητας του μέσου, παράγεται καρβοξυλικό ιόν αντί για καρβοξυλικό οξύ.
Τα τριγλυκερίδια είναι ένας εστέρας που προέρχεται από την αντίδραση μεταξύ μιας γλυκερίνης και των λιπαρών οξέων. Εδώ, ένα μόριο γλυκερίνης συνδυάζεται με τρία μόρια λιπαρών οξέων. Κάθε λιπαρό οξύ έχει μια ομάδα καρβοξυλικού οξέος. Το μόριο της γλυκερόλης έχει τρεις ομάδες υδροξυλίου (-ΟΗ). Ως εκ τούτου, τρία λιπαρά οξέα μπορούν να συνδυαστούν με αυτές τις τρεις υδροξυλομάδες σχηματίζοντας τον εστέρα. Στη σαπωνοποίηση, τρία λιπαρά οξέα διαχωρίζονται από τη γλυκερίνη.
Ο μηχανισμός σαπωνοποίησης περιλαμβάνει τα ακόλουθα βήματα:
- Πυρηνόφιλη επίθεση
- Αποχώρηση κατάργησης ομάδας
- Αποπρωτονίωση
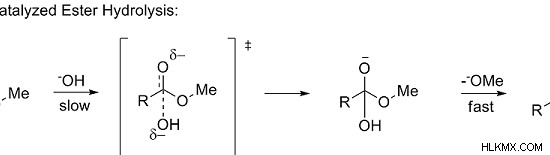
Εικόνα 1:Μηχανισμός σαπωνοποίησης
Γενικά, η χημική αντίδραση μεταξύ οποιουδήποτε λίπους και NaOH είναι η σαπωνοποίηση. Η αντίδραση είναι εξώθερμη, στην οποία απελευθερώνεται θερμότητα στο περιβάλλον. Όταν το σαπούνι σχηματίζεται μέσω σαπωνοποίησης, παραμένει ως εναιώρημα. Στη συνέχεια, το σαπούνι μπορεί να διαχωριστεί μέσω σαπουνιού αλατίσματος (σχηματισμός στερεού σαπουνιού από το εναιώρημα με προσθήκη κοινού αλατιού στο εναιώρημα).
Τι είναι η Εξουδετέρωση
Η αντίδραση εξουδετέρωσης είναι μια χημική αντίδραση μεταξύ ενός οξέος και μιας βάσης που παράγει ένα ουδέτερο διάλυμα. Ένα ουδέτερο διάλυμα θα έχει πάντα pH 7. Αυτή η αντίδραση περιλαμβάνει το συνδυασμό ιόντων Η και ιόντων ΟΗ για να σχηματιστούν μόρια νερού.
Αν το τελικό pH ενός μείγματος αντίδρασης οξέος και βάσης είναι 7, αυτό σημαίνει ότι εδώ έχουν αντιδράσει ίσες ποσότητες ιόντων Η και ΟΗ (για να σχηματιστεί ένα μόριο νερού, ένα Η απαιτούνται ιόν και ένα ιόν ΟΗ). Τα οξέα και οι βάσεις που αντέδρασαν μπορεί να είναι είτε ισχυρά είτε αδύναμα. Οι αντιδράσεις ποικίλλουν ανάλογα με αυτό το γεγονός.
Εξουδετέρωση ισχυρού οξέος-ισχυρής βάσης
- Τα ισχυρά οξέα και οι ισχυρές βάσεις διαχωρίζονται πλήρως σε ιόντα σε υδατικό μέσο. Ως εκ τούτου, απελευθερώνουν όλα τα πιθανά ιόντα Η και ΟΗ στο μέσο.
Εξουδετέρωση ασθενούς οξέος-ασθενούς βάσης
- Αυτός ο τύπος αντίδρασης δεν δίνει πλήρη εξουδετέρωση επειδή τα αδύναμα οξέα και οι ασθενείς βάσεις δεν διασπώνται πλήρως στα ιόντα τους. Ως εκ τούτου, ένα ασθενές οξύ δεν μπορεί να εξουδετερωθεί από μια ασθενή βάση και το αντίστροφο.
Εξουδετέρωση ασθενούς βάσης με ισχυρό οξύ
- Η εξουδετέρωση ενός ασθενούς οξέος με ισχυρή βάση δίνει στο μέσο pH υψηλότερο από 7.
Ισχυρή εξουδετέρωση ασθενούς βάσης σε οξύ
- Η εξουδετέρωση ενός ισχυρού οξέος με ασθενή βάση έχει ως αποτέλεσμα χαμηλό pH από 7.

Εικόνα 2:Εκτέλεση αντίδρασης οξέος-βάσης
Διαφορά μεταξύ σαπωνοποίησης και εξουδετέρωσης
Ορισμός
Σαπωνοποίηση: Η σαπωνοποίηση είναι μια διαδικασία κατά την οποία τα τριγλυκερίδια αντιδρούν με το υδροξείδιο του νατρίου ή του καλίου για να παράγουν γλυκερίνη και ένα άλας λιπαρού οξέος που ονομάζεται «σαπούνι».
Εξουδετέρωση: Μια αντίδραση εξουδετέρωσης είναι μια χημική αντίδραση μεταξύ ενός οξέος και μιας βάσης που παράγει ένα ουδέτερο διάλυμα (pH=7).
Αρχή
Σαπωνοποίηση: Η σαπωνοποίηση περιλαμβάνει τη διάσπαση ενός εστέρα σε αλκοόλη και καρβοξυλικό ιόν.
Εξουδετέρωση: Η εξουδετέρωση περιλαμβάνει το σχηματισμό ουδέτερου μέσου μετά τη χημική αντίδραση.
Τελικά προϊόντα
Σαπωνοποίηση: Η σαπωνοποίηση δίνει γλυκερίνη και ένα άλας λιπαρού οξέος (σαπούνι).
Εξουδετέρωση: Η εξουδετέρωση δίνει αλάτι και νερό.
Χημική Αντίδραση
Σαπωνοποίηση: Η σαπωνοποίηση περιλαμβάνει την αντίδραση μεταξύ ενός εστέρα και υδροξειδίου του νατρίου ή του καλίου παρουσία νερού.
Εξουδετέρωση: Η εξουδετέρωση περιλαμβάνει την αντίδραση μεταξύ ενός οξέος (ισχυρού ή ασθενούς) και μιας βάσης (ισχυρής ή ασθενής).
Τελικό αποτέλεσμα
Σαπωνοποίηση: Η σαπωνοποίηση σχηματίζει το σαπούνι ως εναιώρημα το οποίο μπορεί να διαχωριστεί με αλάτισμα από το σαπούνι.
Εξουδετέρωση: Η εξουδετέρωση σχηματίζει ένα μέσο με pH 7.
Συμπέρασμα
Η σαπωνοποίηση είναι βασικά ο σχηματισμός σαπουνιού. Αυτό περιλαμβάνει τη διάσπαση ενός εστέρα σε αλκοόλη και καρβοξυλικό οξύ (σε ένα βασικό μέσο σχηματίζεται καρβοξυλικό ιόν). Η εξουδετέρωση, από την άλλη πλευρά, είναι ο σχηματισμός ενός ουδέτερου μέσου μετά την αντίδραση μεταξύ ενός οξέος και μιας βάσης. Η κύρια διαφορά μεταξύ σαπωνοποίησης και εξουδετέρωσης είναι ότι η σαπωνοποίηση περιλαμβάνει τη διάσπαση ενός εστέρα σε αλκοόλη και καρβοξυλικό ιόν, ενώ η εξουδετέρωση περιλαμβάνει το σχηματισμό ενός ουδέτερου μέσου μετά τη χημική αντίδραση.
Αναφορά:
1. Helmenstine, Anne Marie. «Ορισμός και αντίδραση σαπωνοποίησης». ThoughtCo, 3 Οκτωβρίου 2017, Διαθέσιμο εδώ.
2. Libretexts. "Σαπωνοποίηση." Chemistry LibreTexts, Libretexts, 21 Ιουλίου 2016, Διαθέσιμο εδώ.
3. Helmenstine, Anne Marie. «Ορισμός εξουδετέρωσης». ThoughtCo, 26 Απριλίου 2016, Διαθέσιμο εδώ.
Εικόνα Ευγενική προσφορά:
1. "Wikipedia υδρόλυση εστέρων." Από Chem540grp5f08 – Ίδιο έργο (Δημόσιος Τομέας) μέσω Commons Wikimedia
2. "Τιτλοδότηση" Από τον Jfreyre~commonswiki υποτίθεται- Αναλαμβάνεται δική του εργασία (βάσει αξιώσεων πνευματικών δικαιωμάτων) (CC BY-SA 2.5) μέσω Commons Wikimedia