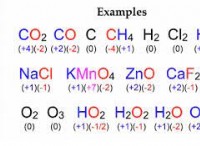
Ποιος είναι ο αριθμός οξείδωσης του υδρογόνου στο HCl;
* χλώριο (cl) είναι πιο ηλεκτροαρνητικό από το υδρογόνο (Η). Αυτό σημαίνει ότι το χλώριο έχει ισχυρότερη έλξη στα κοινόχρηστα ηλεκτρόνια του δεσμού Η-CL.
* Ηλεκτροργατιστικότητα Καθορίζει τον τρόπο με τον οποίο τα κοινόχρηστα ηλεκτρόνια "εκχωρούνται" για λόγους οξείδωσης. Δεδομένου ότι το χλώριο είναι περισσότερο ηλεκτροαρνητικό, παίρνει εκχωρηθεί και τα δύο ηλεκτρόνια από τον δεσμό.
* Αυτό αφήνει το υδρογόνο με ένα λιγότερο ηλεκτρόνιο από την ουδέτερη κατάσταση του, δίνοντάς του έναν αριθμό οξείδωσης +1 .