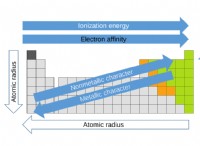
Ποια κατηγορία στοιχείων στον περιοδικό πίνακα τείνει να δημιουργεί αρνητικά φορτισμένα ιόντα;
Εδώ είναι γιατί:
* Ηλεκτροργατιστικότητα: Τα μη μέταλλα έχουν γενικά υψηλότερη ηλεκτροαρνητικότητα από τα μέταλλα. Αυτό σημαίνει ότι έχουν ισχυρότερη έλξη για τα ηλεκτρόνια.
* ηλεκτρόνια σθένους: Τα μη μέταλλα έχουν συνήθως μεγάλο αριθμό ηλεκτρόνων σθένους (ηλεκτρόνια στο εξωτερικό κέλυφος). Τείνουν να κερδίζουν ηλεκτρόνια για να επιτύχουν ένα σταθερό οκτάτο (οκτώ ηλεκτρόνια) στο εξωτερικό κέλυφος τους.
* Σχηματισμός ανιόντων: Κερδίζοντας ηλεκτρόνια, τα μη μέταλλα αποκτούν αρνητικό φορτίο και γίνονται ανιόντα.
Παραδείγματα μη μεταλλικών που σχηματίζουν ανιόντα:
* αλογόνα (ομάδα 17): Το φθόριο (F-), το χλώριο (cl-), το βρώμιο (BR-), το ιώδιο (i-)
* οξυγόνο (O-2):
* θείο (S-2):
* αζώτου (N-3):