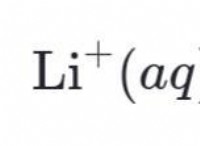Είναι οι ιδιότητες των μεμονωμένων ατόμων και ενώσεων που κάνουν είναι πάντα πολύ παρόμοιες;
* Χημική σύνδεση: Όταν τα άτομα συνδυάζονται για να σχηματίσουν ενώσεις, υποβάλλονται σε χημική σύνδεση. Αυτό περιλαμβάνει την ανταλλαγή ή τη μεταφορά ηλεκτρονίων, τα οποία μεταβάλλουν δραματικά την ηλεκτρονική δομή των ατόμων. Αυτή η αλλαγή στην ηλεκτρονική δομή επηρεάζει άμεσα τις φυσικές και χημικές ιδιότητες της ένωσης.
* Αναδυόμενες ιδιότητες: Οι ενώσεις συχνά εμφανίζουν ιδιότητες που δεν υπάρχουν στα ατομικά άτομα που τα κάνουν. Αυτά ονομάζονται αναδυόμενες ιδιότητες. Για παράδειγμα, το νερό (H₂O) είναι υγρό σε θερμοκρασία δωματίου, ενώ το υδρογόνο (Η) και το οξυγόνο (Ο) είναι και τα δύο αέρια. Οι μοναδικές ιδιότητες του νερού προκύπτουν από την ισχυρή δέσμευση υδρογόνου μεταξύ των μορίων του, μιας ιδιότητας που δεν υπάρχει στα ατομικά άτομα.
* Τύποι σύνδεσης: Ο τύπος του χημικού δεσμού που σχηματίζεται μεταξύ των ατόμων (ιοντικών, ομοιοπολικών, μεταλλικών) επηρεάζει σημαντικά τις ιδιότητες της ένωσης. Για παράδειγμα, οι ιοντικές ενώσεις όπως το χλωριούχο νάτριο (NaCl) έχουν υψηλά σημεία τήξης και είναι καλοί αγωγοί ηλεκτρικής ενέργειας όταν διαλύονται σε νερό, ενώ οι ομοιοπολικές ενώσεις όπως το νερό (H₂O) έχουν χαμηλότερα σημεία τήξης και είναι γενικά κακοί αγωγοί.
Παραδείγματα:
* νάτριο (Na) έναντι χλωριούχου νατρίου (NaCl): Το νάτριο είναι ένα εξαιρετικά αντιδραστικό μέταλλο, ενώ το χλωριούχο νάτριο (επιτραπέζιο άλας) είναι μια σταθερή, μη αντιδραστική ένωση.
* Carbon (C) εναντίον Diamond &Graphite: Ο άνθρακας είναι ένα ευπροσάρμοστο στοιχείο, αλλά οι ιδιότητές του αλλάζουν δραματικά με βάση τον τρόπο με τον οποίο τα άτομα συνδέονται μαζί. Το Diamond είναι εξαιρετικά σκληρό και διαφανές, ενώ ο γραφίτης είναι μαλακός και μαύρος.
Συνοπτικά, ενώ οι ιδιότητες των ατόμων συμβάλλουν στις συνολικές ιδιότητες των ενώσεων που σχηματίζουν, η χημική σύνδεση και οι αναδυόμενες ιδιότητες δημιουργούν νέα και συχνά ξεχωριστά χαρακτηριστικά.