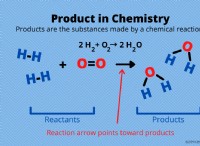
Η σειρά ομολόγων ενός ομοπυρηνικού διατομικού μορίου μπορεί να μειωθεί.
* Αύξηση του αριθμού των ηλεκτρονίων αντιβρωμιών: Τα ηλεκτρόνια αντιβόνωσης αποδυναμώνουν τον δεσμό μεταξύ των ατόμων. Η προσθήκη περισσότερων ηλεκτρόνων σε τροχιακά αντιβασιλέα θα μειώσει τη σειρά δεσμών.
* μείωση του αριθμού των ηλεκτρονίων συγκόλλησης: Τα ηλεκτρόνια συγκόλλησης ενισχύουν τον δεσμό. Η αφαίρεση των ηλεκτρονίων από τα τροχιακά συγκόλλησης θα μειώσει τη σειρά δεσμών.
* Αύξηση της απόστασης μεταξύ των πυρήνων: Καθώς οι πυρήνες κινούνται περισσότερο, η επικάλυψη μεταξύ των ατομικών τροχιακών μειώνεται, οδηγώντας σε ασθενέστερους δεσμούς και χαμηλότερη σειρά δεσμών. Αυτό μπορεί να προκληθεί από παράγοντες όπως:
* Αύξηση του μεγέθους των ατόμων: Τα μεγαλύτερα άτομα έχουν περισσότερα διάχυτα τροχιακά, οδηγώντας σε ασθενέστερη επικάλυψη.
* Προσθήκη περισσότερων κελυφών ηλεκτρονίων: Τα εξωτερικά ηλεκτρόνια είναι περαιτέρω από τον πυρήνα, οδηγώντας σε ασθενέστερους δεσμούς.
* Αύξηση του αριθμού των ηλεκτρονίων: Ενώ αυτό συνήθως αυξάνει την σειρά δεσμών, εάν τα προστιθέμενα ηλεκτρόνια τοποθετηθούν σε τροχιακά αντιβόου, θα μειώσουν τη σειρά δεσμών.
Εδώ είναι ένα παράδειγμα:
Εξετάστε το διατομικό μόριο αζώτου, n 2 . Έχει τριπλό δεσμό (σειρά δεσμού =3) λόγω 10 ηλεκτρόνων σε τροχιακά συγκόλλησης και 4 ηλεκτρόνια σε τροχιακά αντιβασιόν. Αν επρόκειτο να προσθέσουμε δύο ακόμη ηλεκτρόνια, θα καταλάβαιναν τα τροχιακά αντιβόθη, μειώνοντας τη σειρά των δεσμών σε 2 και αποδυναμώνουν τον δεσμό.
Συνοπτικά: Η σειρά δεσμού ενός ομοπυρηνικού διατομικού μορίου μπορεί να μειωθεί από παράγοντες που αποδυναμώνουν τον δεσμό, συμπεριλαμβανομένης της αύξησης του αριθμού των ηλεκτρονίων αντισυμβαλλομένων, μειώνοντας τον αριθμό των ηλεκτρονίων συγκόλλησης ή την αύξηση της απόστασης μεταξύ των πυρήνων.