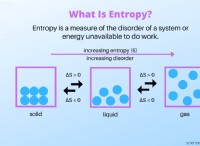
Τι πρέπει να ξεπεραστεί για ένα στερεό υγρό και αέριο αλλαγής;
Εδώ είναι μια κατανομή:
* στερεό έως υγρό (τήξη): Για να λιώσει ένα στερεό, πρέπει να προσθέσετε αρκετή ενέργεια (συνήθως θερμαίνετε) για να σπάσετε τους άκαμπτους δεσμούς που κρατούν τα σωματίδια μαζί. Αυτό επιτρέπει στα σωματίδια να κινούνται πιο ελεύθερα, με αποτέλεσμα μια υγρή κατάσταση.
* υγρό σε αέριο (βρασμός/εξάτμιση): Για να εξατμίσετε ένα υγρό, πρέπει να προσθέσετε ακόμα περισσότερη ενέργεια για να ξεπεράσετε τις ασθενέστερες ελκυστικές δυνάμεις μεταξύ των σωματιδίων. Αυτό τους επιτρέπει να ξεφύγουν από την επιφάνεια του υγρού και να εισέλθουν στην αέρια κατάσταση, όπου κινούνται πολύ πιο ελεύθερα και ανεξάρτητα.
* ΑΕΤΕΣ ΣΤΟ ΥΙΟΚΤΗΡΙΟ (συμπύκνωση): Το αντίστροφο του βρασμού, αυτή η διαδικασία περιλαμβάνει την αφαίρεση ενέργειας από το αέριο. Τα σωματίδια επιβραδύνουν, οι ελκυστικές δυνάμεις γίνονται ισχυρότερες και συναντιούνται για να σχηματίσουν ένα υγρό.
* υγρό έως στερεό (κατάψυξη): Παρόμοια με τη συμπύκνωση, αυτό απαιτεί την αφαίρεση ενέργειας από το υγρό για να επιβραδύνει τα σωματίδια προς τα κάτω. Αυτό επιτρέπει στις ελκυστικές δυνάμεις να στερεοποιήσουν τη δομή, σχηματίζοντας ένα στερεό.
Συνοπτικά, η ποσότητα της παρούσας ενέργειας καθορίζει την κατάσταση της ύλης. Η προσθήκη ενέργειας επιτρέπει στα σωματίδια να κινούνται πιο ελεύθερα, ενώ η αφαίρεση της ενέργειας περιορίζει την κίνηση τους.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σχετικά με συγκεκριμένες ιδιότητες όπως η πίεση και η θερμοκρασία ή οι μοριακές αλληλεπιδράσεις που εμπλέκονται!