Ποιο είναι το παράδειγμα ενός διαλυτού αλατιού σε ζεστό νερό;
* Χλωριούχο νάτριο (NaCl) :Ενώ το αλάτι του τραπεζιού είναι αρκετά διαλυτό τόσο σε ζεστό όσο και σε κρύο νερό, είναι πιο διαλυτό σε ζεστό νερό.
* Νιτρικό κάλιο (KNO3) :Αυτό το αλάτι παρουσιάζει σημαντική αύξηση της διαλυτότητας καθώς αυξάνεται η θερμοκρασία του νερού.
* Χλωριούχο ασβέστιο (CaCl2) :Συνήθως χρησιμοποιείται για την αποδέσμευση, η διαλυτότητα του χλωριούχου ασβεστίου αυξάνεται σημαντικά με τη θερμοκρασία.
* Δενεροξονικό νάτριο (NAHCO3) :Επίσης γνωστή ως σόδα ψησίματος, η διαλυτότητα της αυξάνεται αισθητά σε ζεστό νερό.
Γιατί μερικά άλατα είναι πιο διαλυτά σε ζεστό νερό;
Η διαλυτότητα των αλάτων επηρεάζεται από διάφορους παράγοντες, όπως:
* Θερμοκρασία: Καθώς αυξάνεται η θερμοκρασία, τα μόρια στο νερό κινούνται ταχύτερα, αυξάνοντας την κινητική τους ενέργεια. Αυτό διευκολύνει τα μόρια του νερού να σπάσουν τους ιοντικούς δεσμούς που κρατούν τους κρυστάλλους αλατιού μαζί.
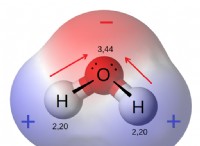
* πολικότητα: Το νερό είναι ένας πολικός διαλύτης, που σημαίνει ότι έχει θετικό και αρνητικό τέλος. Αυτό του επιτρέπει να αλληλεπιδρά με τα ιόντα σε κρυστάλλους αλατιού, να τα απομακρύνει και να τα διαλύει.
* εντροπία: Η αύξηση της εντροπίας (διαταραχή) που συμβαίνει όταν ένα αλάτι διαλύεται στο νερό είναι επίσης μια κινητήρια δύναμη για τη διαλυτότητα.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σχετικά με ένα συγκεκριμένο αλάτι!