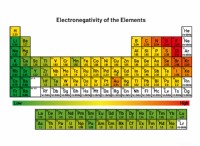
Ποιο καθορίζει την αντιδραστικότητα των στοιχείων;
* Διαμόρφωση ηλεκτρονίων: Η διάταξη των ηλεκτρονίων σε τα κελύφη και τα υποβρύχια ενός ατόμου υπαγορεύει πόσο εύκολα ένα άτομο θα κερδίσει, θα χάσει ή θα μοιραστεί ηλεκτρόνια για να επιτύχει μια σταθερή διαμόρφωση. Τα στοιχεία με σχεδόν πλήρες ή σχεδόν άδειο εξωτερικό κέλυφος τείνουν να είναι εξαιρετικά αντιδραστικά, επιδιώκοντας να ολοκληρώσουν το εξωτερικό τους κέλυφος.
* Ηλεκτροργατιστικότητα: Αυτό είναι ένα μέτρο της ικανότητας ενός ατόμου να προσελκύει ηλεκτρόνια σε χημικό δεσμό. Τα εξαιρετικά ηλεκτροαρνητικά στοιχεία κερδίζουν εύκολα ηλεκτρόνια, καθιστώντας τα αντιδραστικά.
* ενέργεια ιονισμού: Η ενέργεια που απαιτείται για την απομάκρυνση ενός ηλεκτρονίου από ένα άτομο. Στοιχεία με χαμηλή ενέργεια ιονισμού χάνουν εύκολα ηλεκτρόνια, καθιστώντας τα αντιδραστικά.
* συγγένεια ηλεκτρονίων: Η αλλαγή ενέργειας όταν ένα ηλεκτρόνιο προστίθεται σε ένα ουδέτερο άτομο. Στοιχεία με υψηλή συγγένεια ηλεκτρονίων κερδίζουν εύκολα ηλεκτρόνια, καθιστώντας τα αντιδραστικά.
* Μεταλλικός χαρακτήρας: Τα μέταλλα τείνουν να είναι πιο δραστικά από τα μη μέταλλα. Ο μεταλλικός χαρακτήρας αυξάνεται καθώς κινείστε προς τα κάτω και προς τα αριστερά στον περιοδικό πίνακα.
Ας το καταρρίψουμε περαιτέρω:
Αντιδραστικότητα των μετάλλων:
* Μέταλλα με ενέργειες χαμηλού ιονισμού χάνουν εύκολα ηλεκτρόνια και σχηματίζουν θετικά ιόντα (κατιόντα), καθιστώντας τα εξαιρετικά αντιδραστικά. Παραδείγματα:Αλκαλικά μέταλλα (ομάδα 1) και μέταλλα αλκαλικής γης (Ομάδα 2).
* μέταλλα με υψηλό βαθμό μεταλλικού χαρακτήρα είναι επίσης εξαιρετικά αντιδραστικά, λόγω της τάσης τους να δώσουν ηλεκτρόνια.
Αντιδραστικότητα μη μεταλλικών:
* Μη μέταλλα με υψηλή ηλεκτροαρνητικότητα Κερδίστε εύκολα ηλεκτρόνια και σχηματίζουν αρνητικά ιόντα (ανιόντα), καθιστώντας τα εξαιρετικά αντιδραστικά. Παραδείγματα:αλογόνα (ομάδα 17).
* Μη μέταλλα με υψηλή συγγένεια ηλεκτρονίων Επίσης, κερδίζετε εύκολα ηλεκτρόνια.
Περιοδικές τάσεις:
* Η αντιδραστικότητα αυξάνει την κίνηση προς τα κάτω μια ομάδα Για τα μέταλλα, καθώς τα εξωτερικά ηλεκτρόνια γίνονται περαιτέρω από τον πυρήνα και είναι ευκολότερο να αφαιρεθούν.
* Η αντιδραστικότητα μειώνεται με τη μετακίνηση μιας ομάδας Για τα μη μέταλλα, καθώς τα εξώτατα ηλεκτρόνια γίνονται πιο κοντά στον πυρήνα και πιο δύσκολο να κερδίσουν.
* Η αντιδραστικότητα μειώνεται με τη μετακίνηση δεξιά σε μια περίοδο Και για τα μέταλλα και τα μη μέταλλα, καθώς αυξάνεται το πυρηνικό φορτίο και η έλξη στα ηλεκτρόνια ενισχύεται.
Εξαιρέσεις και σκέψεις:
* ευγενή αέρια γενικά δεν είναι αντιδραστικά λόγω των σταθερών, πλήρους εξωτερικών κελυφών ηλεκτρονίων.
* Μεταβατικά μέταλλα έχουν μεταβλητή αντιδραστικότητα ανάλογα με την κατάσταση οξείδωσης και άλλους παράγοντες.
* Η αντιδραστικότητα μπορεί επίσης να επηρεαστεί από παράγοντες όπως η θερμοκρασία, η πίεση και η παρουσία άλλων στοιχείων.
Επομένως, η κατανόηση της αλληλεπίδρασης αυτών των παραγόντων είναι ζωτικής σημασίας για την πρόβλεψη και την εξήγηση της αντιδραστικότητας των στοιχείων.