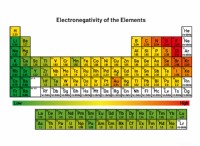
Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ των μεταλλικών μετάλλων μη μέταλλα;
Ομοίες και διαφορές μεταξύ μετάλλων, μεταλλοειδών και μη μεταλλικών:
ομοιότητες:
* Όλα είναι στοιχεία: Όλοι βρίσκονται στον περιοδικό πίνακα και αποτελούνται μόνο από έναν τύπο ατόμου.
* μπορεί να σχηματίσει ενώσεις: Μπορούν να συνδυαστούν με άλλα στοιχεία για να σχηματίσουν διάφορες ενώσεις.
* υπάρχουν σε διαφορετικές καταστάσεις ύλης: Ορισμένα είναι στερεά, υγρά ή αέριο σε θερμοκρασία δωματίου.
Διαφορές:
1. Φυσικές ιδιότητες:
| Ιδιοκτησία | Μέταλλα | Μεταλλοειδή | Μη μέταλλα |
| --- | --- | --- | --- |
| εμφάνιση | Λαμπερό, λαμπερό | Μπορεί να είναι λαμπερό ή θαμπό | Θαμπό, εύθραυστο |
| Malleability | Λουλούδια (μπορεί να σφυρηλατηθεί σε φύλλα) | Μερικοί είναι, μερικοί δεν είναι | Δεν είναι εύπλαστο |
| ολκιμότητα | Όλκιμο (μπορεί να ληφθεί σε καλώδια) Μερικοί είναι, μερικοί δεν είναι | Όχι όλκιμο |
| αγωγιμότητα | Καλοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας | Ημιαγωγοί (διεξαγωγή ηλεκτρικής ενέργειας υπό συγκεκριμένες συνθήκες) Κακοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας |
| πυκνότητα | Γενικά υψηλή | Μεταβλητή | Γενικά χαμηλά |
2. Χημικές ιδιότητες:
| Ιδιοκτησία | Μέταλλα | Μεταλλοειδή | Μη μέταλλα |
| --- | --- | --- | --- |
| Οξείδωση | Εύκολα οξειδώνεται (χάνουν ηλεκτρόνια) Μπορεί να λειτουργήσει ως μέταλλα ή μη μέταλλα ανάλογα με τις συνθήκες Μπορεί να κερδίσει ηλεκτρόνια εύκολα (μείωση)
| Αντιδραστικότητα | Εξαιρετικά αντιδραστικό (ειδικά αλκαλικά μέταλλα) Μεταβλητή | Λιγότερο αντιδραστικό |
| ιόντα | Σχηματίζουν θετικά ιόντα (κατιόντα) Μπορεί να σχηματίσει τόσο θετικά όσο και αρνητικά ιόντα | Σχηματίζουν αρνητικά ιόντα (ανιόντα)
3. Παραδείγματα:
* μέταλλα: Σίδηρος, χαλκός, χρυσός, ασήμι, αλουμίνιο, νάτριο, κάλιο
* Metalloids: Πυρίτιο, γερμάνιο, αρσενικό, αντιμόνιο, Tellurium
* Μη μετάλλια: Οξυγόνο, άζωτο, άνθρακα, θείο, φωσφόρος, χλώριο, βρωμίρο, ιώδιο
4. Χρήσεις:
* μέταλλα: Κατασκευή, ηλεκτρονικά, κοσμήματα, μεταφορά, παραγωγή ενέργειας
* Metalloids: Ημιαγωγοί σε ηλεκτρονικά, υπολογιστές, ηλιακούς συλλέκτες
* Μη μετάλλια: Απαραίτητο για τη ζωή (οξυγόνο, άζωτο), βιομηχανικές χημικές ουσίες (χλώριο), φαρμακευτικά προϊόντα
Συνοπτικά: Τα μέταλλα είναι γενικά καλοί αγωγοί, εύπλαστες και όλκιμοι. Τα μη μέταλλα είναι κακοί αγωγοί, εύθραυστοι και συχνά σχηματίζουν αρνητικά ιόντα. Τα μεταλλοειδή έχουν ιδιότητες που βρίσκονται κάπου μεταξύ εκείνων των μετάλλων και των μη μεταλλικών, καθιστώντας τους χρήσιμες ως ημιαγωγούς.