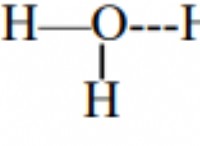Διαλύεται το λίθιο σε άλλους διαλύτες;
Εδώ είναι γιατί:
* υψηλή αντιδραστικότητα: Το λίθιο είναι ένα εξαιρετικά αντιδραστικό αλκαλικό μέταλλο. Αντιδρά βίαια με νερό, σχηματίζοντας υδροξείδιο του λιθίου και αέριο υδρογόνου. Αυτή η αντίδραση είναι εξωθερμική και μπορεί να είναι εκρηκτική.
* Ισχυρή μεταλλική σύνδεση: Το λίθιο έχει ισχυρή μεταλλική συγκόλληση, γεγονός που καθιστά δύσκολη την διάσπαση των ατόμων του και τη διαλύστε τους σε έναν διαλύτη.
* Περιορισμένη διαλυτότητα σε υγρή αμμωνία: Το λίθιο μπορεί να διαλύεται σε υγρή αμμωνία, αλλά αυτή είναι μια εξειδικευμένη περίπτωση. Σχηματίζει ένα μπλε διάλυμα λόγω των διαλυμένων ηλεκτρόνων.
Επομένως, το λίθιο δεν διαλύεται στους πιο κοινούς διαλύτες. Η αντιδραστικότητα του καθιστά ακατάλληλο για διάλυση στα περισσότερα υγρά μέσα.