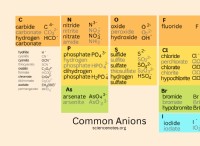
Ποιος τύπος στοιχείων κάνει αρνητικά ιόντα;
* Ηλεκτροργατιστικότητα: Τα μη μέταλλα έχουν υψηλότερη ηλεκτροαρνητικότητα από τα μέταλλα. Αυτό σημαίνει ότι έχουν ισχυρότερη έλξη για τα ηλεκτρόνια.
* Διαμόρφωση ηλεκτρονίων: Τα μη μέταλλα έχουν συνήθως ένα σχεδόν πλήρες εξωτερικό κέλυφος ηλεκτρονίων. Κερδίζοντας ένα ή περισσότερα ηλεκτρόνια, μπορούν να επιτύχουν μια σταθερή, πλήρη διαμόρφωση εξωτερικού κελύφους.
Παράδειγμα:
* Το χλώριο (CL) είναι μη μέταλλο. Έχει 7 ηλεκτρόνια στο εξωτερικό κέλυφος του. Με την απόκτηση ενός ηλεκτρονίου, γίνεται ένα ιόν χλωριούχου (cl-), με ένα πλήρες εξωτερικό κέλυφος 8 ηλεκτρονίων.
Βασικό σημείο: Ο σχηματισμός αρνητικών ιόντων ονομάζεται σχηματισμός ανιόντων .