Πώς οδήγησε η αναζήτηση της Φιλοσοφικής Λίθου στην Ανακάλυψη του Φωσφόρου;
Η μείωση των ούρων, που επιτεύχθηκε στην αναζήτηση της φιλοσοφικής πέτρας, οδήγησε στην ανακάλυψη του φωσφόρου, ενός στοιχείου με μια απόκοσμη λάμψη—και ενός από τα θεμελιώδη στοιχεία που συνθέτουν τη ζωή στη Γη.
Η τέχνη της Αλχημείας και ο θρύλος της Φιλοσοφικής πέτρας δεν είναι μυστήριο για εμάς. Παντού, από τον «Αλχημιστή» έως τον «Χάρι Πότερ», συναντάμε αναφορές στη φιλοσοφική πέτρα - το ελιξίριο της ζωής που μπορεί να μεταμορφώσει οποιοδήποτε μέταλλο σε καθαρό χρυσό. Τον 17ο αιώνα, πολλοί επιστήμονες και φιλόσοφοι, συμπεριλαμβανομένου του Sir Isaac Newton, ήταν απορροφημένοι σε αυτή τη μυστικιστική τέχνη της πνευματικότητας και της επιστήμης.
Το 1669, ο Γερμανός αλχημιστής Hennig Brandt ξεκίνησε την αναζήτησή του για τη φιλοσοφική πέτρα στο υπόγειο εργαστήριό του στο Αμβούργο της Γερμανίας, χρησιμοποιώντας κάτι πολύ ενδιαφέρον. Παρόλο που η επιδίωξή του δεν οδήγησε στην ανακάλυψη της φιλοσοφικής πέτρας, κατέληξε σε κάτι ακόμα πιο αξιοσημείωτο.

(Φωτογραφία:εικόνες καλωσορίσματος/Wikimedia commons) Hennig Brand
Philosopher’s Stone From Urine?
Το μαγικό συστατικό στην αναζήτηση του Hennig για την πέτρα ήταν τα ούρα . Τότε, τα ούρα ονομάζονταν «χρυσό ρεύμα» λόγω της ομοιότητάς τους με το χρώμα του χρυσού. Το χρυσοκίτρινο χρώμα των ούρων το έκανε μια ενδιαφέρουσα επιλογή μεταξύ των αλχημιστών που αναζητούσαν χρυσό.
Ο Brandt συγκέντρωσε σχεδόν 50 κουβάδες ούρα, πιστεύοντας ότι η φιλοσοφική πέτρα θα μπορούσε να εξαχθεί από αυτά.
Η Συνταγή του Μπραντ για τη Φιλοσοφική Λίθο
Πρώτον, ο Brandt άφησε τα ούρα να σαπίσουν για μέρες στο κελάρι του. Αργότερα, έβρασε τα ταγγισμένα ούρα για να φύγει όλο το νερό, με αποτέλεσμα να σχηματιστεί ένα παχύρρευστο, δύσοσμο, κίτρινο σιρόπι.
Η περαιτέρω θέρμανση οδήγησε στο σχηματισμό ενός κοκκινωπού στρώματος λαδιού. Αφαίρεσε αυτό το λάδι και κράτησε το διάλυμα να κρυώσει. Αυτό είχε ως αποτέλεσμα να σχηματιστεί ένα μαύρο, παχύρρευστο υγρό και ένα λευκό αλμυρό στρώμα κάτω από αυτό.
Ο Μπραντ πέταξε το αλάτι και ανακάτεψε ξανά το μαύρο σιρόπι με το κόκκινο λάδι. Ζέστανε το μείγμα δυνατά για περίπου 16 ώρες, ελπίζοντας ότι θα υλοποιηθεί στη φιλοσοφική πέτρα.
Τελικά, μετά από πολύ αγώνα, παρατήρησε λευκές αναθυμιάσεις να γεμίζουν το θάλαμο, οι οποίες στη συνέχεια ξέσπασαν σε λαμπερές φλόγες με μια συναρπαστική λάμψη. Αργότερα πέρασε την ουσία σε έναν δέκτη με κρύο νερό και παρατήρησε μια λευκή, κηρώδη ουσία να στερεοποιείται μέσα του.
Η ουσία που είχε ανακαλύψει ήταν μαγευτική. Στο σκοτάδι, το λευκό στερεό φαινόταν να λάμπει με ένα αχνό πράσινο φως και όταν έμεινε έξω στον αέρα, φαινόταν να απελευθερώνει έναν λευκό καπνό και να καίει με μια φωτεινή λάμψη.
Περιέγραψε το φαινόμενο ως «κρύα φωτιά» και ονόμασε την ουσία «Φώσφορος» που σήμαινε «Ο Φορέας του Φωτός» (Στα ελληνικά, «phôs» σημαίνει «φως» και «phoros» σημαίνει «κομιστής»).

(Φωτογραφία:εικόνες καλωσορίσματος/Wikimedia Commons) Η Ανακάλυψη του Φωσφόρου. Πίνακας του Τζόζεφ Ράιτ.
Ο Brandt ήταν σίγουρος ότι είχε ανακαλύψει κάτι μεγαλειώδες, αλλά ελάχιστα ήξερε ότι η ανακάλυψή του αργότερα θα μεταμόρφωσε τον κόσμο και όλη τη ζωή σε αυτόν.
Πώς ο Brandt εξήγαγε τον φώσφορο;
Ναι, ο Henning Brandt ανακάλυψε στην πραγματικότητα τον φώσφορο από τα ούρα, αλλά πώς;

Το ανθρώπινο σώμα περιέχει μικρές ποσότητες φωσφόρου, κυρίως στα οστά, τα δόντια και τα ούρα μας.
Όταν ο Brandt εξάτμισε τα ούρα, είχε ως αποτέλεσμα να σχηματιστεί κάτι που ονομάζεται όξινο φωσφορικό νάτριο αμμώνιο. Με περαιτέρω θέρμανση, αυτό μειώθηκε σε φωσφορώδες νάτριο .
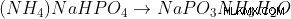
Αργότερα, όταν θερμάνθηκε έντονα η ουσία με ξυλάνθρακα, το φωσφορώδες νάτριο αποσυντέθηκε για να δώσει λευκό φώσφορο και πυροφωσφορικό νάτριο .
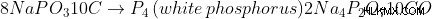
Αυτός ο λευκός φώσφορος είναι αυτό που κατατέθηκε ως η κηρώδης λευκή ουσία.
Σύντομη σημείωση για τον φώσφορο
Ο φώσφορος είναι ένα περίεργο στοιχείο. Είναι ένα από τα θεμελιώδη στοιχεία που συνθέτουν τη ζωή στη Γη, αλλά δεν υπάρχει ως ελεύθερο στοιχείο στη φύση. Ακριβώς όπως ο άνθρακας υπάρχει ως διαμάντι ή γραφίτης, έτσι και ο φώσφορος υπάρχει στη φύση ως αλλότροπα, δηλαδή κόκκινο , λευκό , και μαύρο φώσφορο .
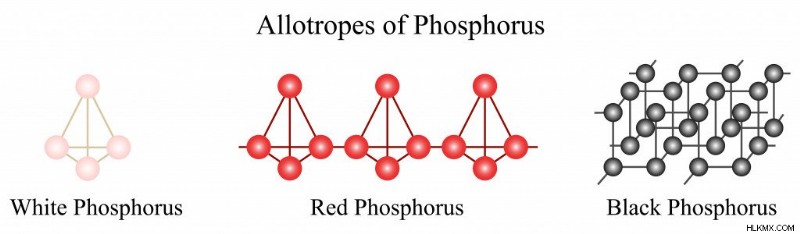
Allotropes of Phosphorus (Photo Credit :Sansanorth/Shutterstock)
Μεταξύ αυτών, ο λευκός και ο κόκκινος φώσφορος είναι αμέταλλα, ενώ ο μαύρος φώσφορος είναι ημι-μέταλλο. Εδώ, έχουμε να κάνουμε με τον λευκό φώσφορο, οπότε ας το συζητήσουμε λεπτομερώς.
Ο λευκός φώσφορος είναι ένα λευκό, κηρώδες στερεό που είναι εξαιρετικά τοξικό και εξαιρετικά αντιδραστικό. Αποτελείται από 4 άτομα φωσφόρου που συγκρατούνται μεταξύ τους με δεσμούς σε σχήμα κάμψης που ονομάζονται «δεσμοί μπανάνας».

Μερικές φορές, ο λευκός φώσφορος μπορεί να φαίνεται ελαφρώς κίτρινος λόγω της παρουσίας ακαθαρσιών. δίνοντάς του το όνομα «κίτρινος φώσφορος». (Πιστωτική φωτογραφία :BXXXD/Wikimedia commons)
What's With All the Glow;
Δύο αξιοσημείωτα χαρακτηριστικά του φωσφόρου κατά την ανακάλυψη του Brandt ήταν η αχνή πράσινη λάμψη του και η λαμπερή φλόγα που εκρήγνυται. Τι τα προκαλεί;
Γιατί λάμπει ο φώσφορος στο σκοτάδι;
Μία από τις πιο εκπληκτικές ιδιότητες του λευκού φωσφόρου είναι η μαγευτική λάμψη του.
Κάθε φορά που ακούμε τον όρο «λάμπει στο σκοτάδι», έρχεται στο μυαλό η εικόνα μιας φωτεινής λάμψης νέον, αλλά η λάμψη του φωσφόρου δεν είναι τόσο διακριτή. Στο σκοτάδι, δείχνει απλώς μια αχνή, γαλαζοπράσινη λάμψη.
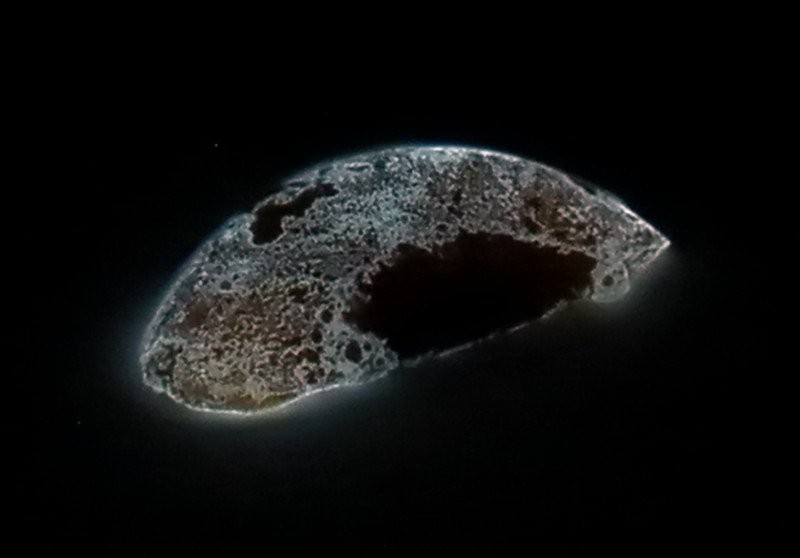
(Φωτογραφία:Endimion17/Wikimedia commons) Η αμυδρή λάμψη του φωσφόρου
Αυτή η λάμψη οφείλεται σε μια χημική αντίδραση που συμβαίνει μεταξύ φωσφόρου και οξυγόνου. Όταν εκτίθεται σε υγρό αέρα , ο λευκός φώσφορος υφίσταται αργή οξείδωση και αντιδρά με τα μόρια οξυγόνου για να απελευθερώσει ενδιάμεσα όπως το P2O2 και HPO . Αυτά τα μόρια είναι υπεύθυνα για την αμυδρή μπλε-πράσινη λάμψη του φωσφόρου.
Όταν η ενέργεια απελευθερώνεται με τη μορφή φωτός κατά τη διάρκεια μιας χημικής αντίδρασης, το φαινόμενο ονομάζεταιχημιφωταύγεια .
Γιατί ο φώσφορος εκρήγνυται σε λαμπερές φλόγες;
Όταν ο Brandt ζέστανε το παρασκεύασμα ούρων του, παρατήρησε μια εκθαμβωτική φωτεινή λάμψη αντί για το αχνό φως, αλλά γιατί;
Όπως αναφέρθηκε προηγουμένως, η αμυδρή λάμψη του φωσφόρου συμβαίνει παρουσία υδρατμών, δηλαδή απαιτεί υγρή ατμόσφαιρα σε θερμοκρασία δωματίου.
Αλλά κατά τη διάρκεια του πειράματος του Brandt, θέρμανε το μείγμα δυνατά για πάνω από 16 ώρες, κάτι που αφαιρούσε το μεγαλύτερο μέρος των υδρατμών.
Ελλείψει υδρατμών, η οξείδωση του φωσφόρου γίνεται ταχύτερη και πιο σταθερή. Έτσι, η αργή οξείδωση του φωσφόρου σταδιακά δίνει τη θέση της σε σταθερή καύση .
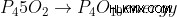
Η καύση του φωσφόρου απελευθερώνει μια καλή ποσότητα θερμότητας και φωτός, με αποτέλεσμα τον σχηματισμό πεντοξειδίου του φωσφόρου, που παρατηρείται ως πυκνό σύννεφο λευκού καπνού πάνω από το δοχείο. Αυτό το αέριο είναι διαβρωτικό και ερεθιστικό.
Καύση Φωσφόρου
Εν ολίγοις, ο λευκός φώσφορος είναι ένα εξαιρετικά αντιδραστικό στοιχείο που αντιδρά αυθόρμητα με τον αέρα σε θερμοκρασία δωματίου. Καθώς η θερμοκρασία αυξάνεται, η αντίδραση γίνεται πιο έντονη και μετατρέπεται από ελαφρύ αναθυμιασμό σε φλογερή έκλαμψη.
Το νερό αναστέλλει την καύση του φωσφόρου, γι' αυτό αποθηκεύουμε φώσφορο στο νερό.
Τι συνέβη μετά την ανακάλυψη του Brandt;
Κατανοώντας ότι είχε αποκαλύψει κάτι υπέροχο, ο Brandt κράτησε την ανακάλυψή του μυστική μέχρι το 1675. Σύντομα, τα νέα της ανακάλυψής του διαδόθηκαν και πολλοί αλχημιστές και επιστήμονες όπως ο Daniel Kraft, ο Johann Kunckel και ο Robert Boyle έκαναν τις δικές τους ανατροπές στη συνταγή του Brandt και ξεκίνησαν παράγοντας φώσφορο.
Τελικά, έναν αιώνα μετά την ανακάλυψη του Brandt, ο Antoine Lavoisier, The Father of Modern Chemistry, αποδέχτηκε τον φώσφορο ως στοιχείο.
Σύντομα, ανακαλύφθηκε ότι τα οστά και τα δόντια ήταν καλύτερη πηγή φωσφόρου από τα ούρα. Έτσι, η εμπορική παραγωγή φωσφόρου ξεκίνησε με τη χρήση οστών ζώων, τα οποία τελικά οδήγησαν στην κατασκευή σπίρτων φωσφόρου.
Η αυξημένη εμπορική χρήση και η μαζική παραγωγή φωσφόρου του έδωσαν σημαντικό ρόλο κατά τη διάρκεια της Βιομηχανικής Επανάστασης.
Το Στοιχείο του Διαβόλου
Μετά από μακροχρόνια χρήση, η τοξικότητα του φωσφόρου ήρθε στο φως όταν οι άνθρωποι που εργάζονταν με φώσφορο άρχισαν να αναπτύσσουν μια παραμόρφωση της γνάθου που ονομάζεται "φωσφορική γνάθο" . Αυτό αργότερα διαπιστώθηκε ότι προκαλείται από τη μακροχρόνια εισπνοή ατμών φωσφόρου, που οδήγησε στην έκπλυση του φωσφόρου στα οστά. Αυτό προκάλεσε οίδημα της γνάθου και χαλάρωση των δοντιών.
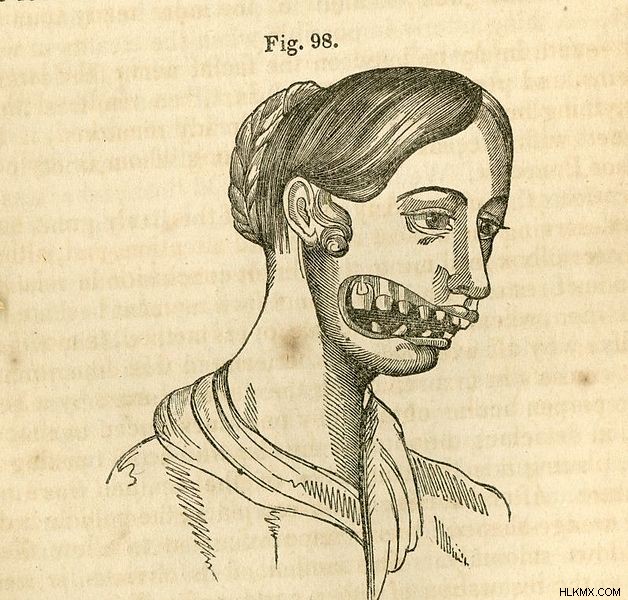
(Φωτογραφία :Mutter/Wikimedia Commons) Phossy Jaw
Η ανακάλυψη της τοξικότητας και του κινδύνου που προκαλεί ο φώσφορος οδήγησε στην άνθηση δύο άλλων αγορών - των όπλων και του πολέμου. Οι βόμβες φωσφόρου και τα χημικά ήταν ένα σημαντικό μέρος του Α' και Β' Παγκοσμίου Πολέμου. Έτσι, ο φώσφορος πήρε το παρατσούκλι "Το Στοιχείο του Διαβόλου".
Ο φώσφορος είναι ένα απαραίτητο στοιχείο που είναι απαραίτητο για τη διατήρηση της ζωής. Από το DNA μας μέχρι το νερό και το έδαφος στη Γη, ο φώσφορος υπάρχει παντού. Τα φυτά χρειάζονται επίσης φώσφορο για καλή ανάπτυξη και υψηλή απόδοση. Αυτός είναι ο λόγος για τον οποίο ο φώσφορος είναι ένα από τα κύρια συστατικά των λιπασμάτων. «Η Πράσινη Επανάσταση», η οποία οδηγήθηκε κυρίως από τα λιπάσματα, ήταν δυνατή μόνο χάρη στον φώσφορο. Ως εκ τούτου, είναι ασφαλές να πούμε ότι ο φώσφορος υπήρξε βασικό στοιχείο σε αμέτρητα σημαντικά γεγονότα σε όλο τον κόσμο.
Μπορούμε όλοι να συμφωνήσουμε ότι μέσω της τυχαίας ανακάλυψης του φωσφόρου, ο Henning Brandt πέτυχε κάτι μνημειώδες και πολύ πιο σημαντικό από την αρχική του αναζήτηση. Όπως μας υπενθυμίζει περίφημα ο Μπομπ Ρος, "Δεν κάνουμε λάθη, απλά ευτυχισμένα μικρά ατυχήματα."