Ποια είναι τα 7 διατομικά στοιχεία; Ορισμός και Λίστα
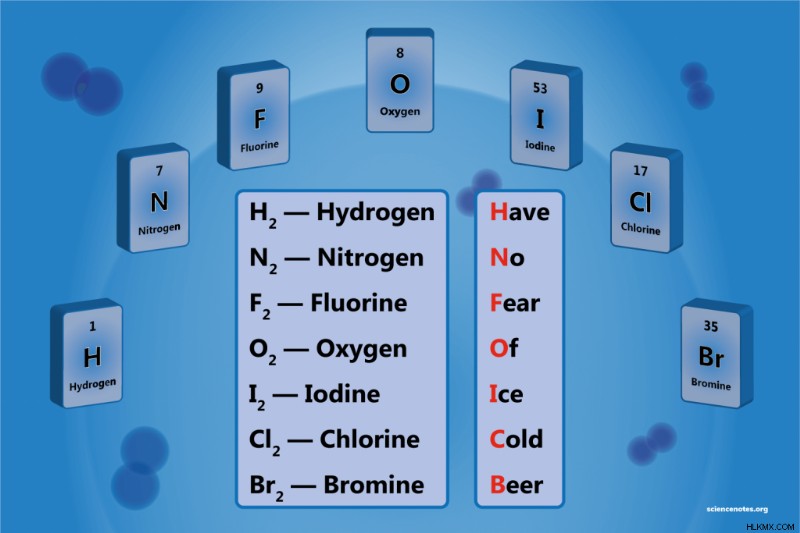
Ένα διατομικό στοιχείο είναι ένα μόριο ενός στοιχείου που αποτελείται από δύο άτομα. Είναι μια μορφή ομοπυρηνικού διατομικού μορίου. Υπάρχουν 7 διατομικά στοιχεία, αλλά μόνο 5 διατομικά στοιχεία σε τυπική θερμοκρασία και πίεση (STP). Τα διατομικά στοιχεία είναι υδρογόνο, άζωτο, οξυγόνο, φθόριο, χλώριο, βρώμιο και ιώδιο.
Λίστα με τα 7 διατομικά στοιχεία
Τα ακόλουθα αέρια 5 στοιχείων είναι διατομικά μόρια σε θερμοκρασία δωματίου και κανονική πίεση:
- Υδρογόνο – H2
- Άζωτο – N2
- Οξυγόνο – O2
- Φθόριο – F2
- Χλώριο – Cl2
Τα ομοπυρηνικά διατομικά αέρια είναι επίσης γνωστά ως «μοριακά αέρια» ή «στοιχειώδη αέρια».
Το βρώμιο και το ιώδιο υπάρχουν συνήθως σε υγρή μορφή, αλλά και ως διατομικά αέρια σε ελαφρώς υψηλότερες θερμοκρασίες, αποτελώντας συνολικά 7 διατομικά στοιχεία.
- Βρώμιο – Br2
- Ιώδιο – I2
Όλα τα διατομικά στοιχεία είναι τύποι μη μετάλλων. Το φθόριο, το χλώριο, το βρώμιο και το ιώδιο είναι όλα αλογόνα. Είναι πιθανό η αστίνη (ατομικός αριθμός 85, σύμβολο στοιχείου At) και η τεννεσίνη (ατομικός αριθμός 117, σύμβολο στοιχείου Ts) να σχηματίζουν διατομικά μόρια, αλλά έχουν παραχθεί ανεπαρκείς ποσότητες για την επαλήθευση αυτής της συμπεριφοράς. Μερικά από αυτά τα στοιχεία σχηματίζουν άλλα σταθερά μόρια. Για παράδειγμα, το οξυγόνο σχηματίζει επίσης όζον (O3 ), το οποίο είναι τριατομικό.
Άλλα στοιχεία μπορούν σχηματίζουν διατομικά μόρια εκτός από τα επτά αυτής της λίστας. Ωστόσο, αυτά τα μόρια δεν είναι πολύ σταθερά, επομένως οι χημικοί τους δεσμοί σπάνε εύκολα. Διφωσφόρος (P2 ), διθείο (S2 ), διλίθιο (Li2 ), και δινάτριο (Na2 ) όλα συμβαίνουν όταν τα στερεά τους εξατμίζονται, αλλά αυτά τα διατομικά στοιχεία υπάρχουν μόνο ως αέρια που επαναπολυμερίζονται όταν ψύχονται. Ditungsten (W2 ) και διμολυβδαίνιο (Mo2 ) συμβαίνουν επίσης. Αυτά τα στοιχεία είναι ενδιαφέροντα γιατί σχηματίζουν εξαπλούς δεσμούς μεταξύ τους στην αέρια φάση! Κάτω από ειδικές συνθήκες, το ρουβίδιο μπορεί να σχηματίσει διρουβίδιο (Rb2 ) και τριρουβίδιο (Rb3 ).
Πώς να θυμάστε τα διατομικά στοιχεία
Μια εύκολη μνημονική συσκευή είναι:
H λεωφόρος N o F αυτί O f I ce C παλιό B eer
Υδρογόνο
Αζωτο
Φθόριο
Οξυγόνο
Ιώδιο
Χλώριο
Βρώμιο
Τα διατομικά στοιχεία είναι το –ine αλογόνα (φθόριο, χλώριο, βρώμιο, ιώδιο) και στοιχεία με –γονίδιο κατάληξη (υδρογόνο, οξυγόνο, άζωτο). Η αστατίνη είναι ένα άλλο αλογόνο, αλλά η συμπεριφορά της δεν είναι γνωστή.
Άλλα μνημονικά είναι τα BrINClHOF (προφέρεται «Brinklehof»), HOFBrINCl (προφέρεται «Hofbrinkle») και HONClBrIF (προφέρεται «Honkelbrif»). Αυτές οι μνημονικές συσκευές βοηθούν στην ανάκληση ποια στοιχεία είναι διατομικά, αλλά όχι η σειρά τους στον περιοδικό πίνακα.
Άλλα διατομικά μόρια
Ενώ τα διατομικά στοιχεία είναι ασυνήθιστα, τα διατομικά μόρια εμφανίζονται εύκολα. Κοινά παραδείγματα περιλαμβάνουν το χλωριούχο νάτριο (NaCl), το μονοξείδιο του άνθρακα (CO) και το μονοξείδιο του αζώτου (ΝΟ). Περίπου το 99% της ατμόσφαιρας της Γης αποτελείται από διατομικά μόρια (άζωτο και οξυγόνο).
Αναφορές
- Huber, K. P.; Herzberg, G. (1979). Μοριακά Φάσματα και Μοριακή Δομή IV. Σταθερές Διατομικών Μορίων . Νέα Υόρκη:Van Nostrand:Reinhold.
- Sherman, Alan (1992). Η χημεία και ο κόσμος μας που αλλάζει . Prentice Hall. ISBN 9780131315419.
- Lu, Z.W.; Wang, Q.; Αυτός, W.M.; Μα, Ζ.Γ. (Ιούλιος 1996). «Νέες παραμετρικές εκπομπές σε διατομικά μόρια νατρίου». Εφαρμοσμένη Φυσική Β. 63 (1):43–46. doi:10.1007/BF01112836




